题目内容
17.某学习小组开展下列实验探究活动:(1)装置A中反应的化学方程式为CaSO3+2HCl=CaCl2+SO2↑+H2O.
(2)利用装置A中产生的气体设计实验证明+4价硫具有氧化性:将SO2通入氢硫酸溶液或者硫化钠溶液中,出现淡黄色沉淀,证明+4价硫具有氧化性.
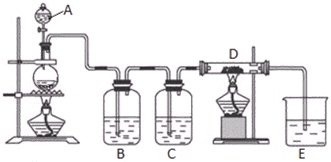
(3)选用下面的装置和药品探究亚硫酸与次氯酸的酸性强弱.
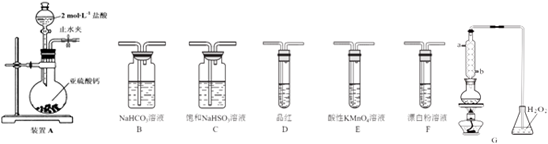
装置连接顺序为ACBEDF,其中装置C的作用是除去HCl气体,通过当D中品红不褪色,F中出现白色沉淀现象即可证明亚硫酸的酸性强于次氯酸.
(4)利用G装置可测定装置A残液中SO2的含量.量取1.00mL残液于烧瓶中,加适量的水稀释,加热使SO2全部逸出并与锥形瓶中H2O2完全反应(SO2+H2O2=H2SO4,然后用0.1000mo1/L-1 NaOH标准溶液进行滴定,至终点时消耗NaOH溶液20.00mL.
①G中球形冷凝管的冷凝水进口为b(填“a”或“b”).
②残液中SO2含量为64.00g.L-1.
③经多次测定发现,测定值始终高于实验值,则其原因是残液中有剩余的盐酸(或过氧化氢),导致实验中消耗的氢氧化钠的量偏多.
(5)设计实验证明H2SO3为二元弱酸:用0.10mol﹒L-1NaOH溶液来滴定10mL0.05mol﹒L-1H2SO3溶液,消耗NaOH溶液的体积为10mL,即证明为二元酸或在滴有酚酞的10mL0.05mol﹒L-1H2SO3溶液中,滴加10mL0.10mol﹒L-1NaOH溶液后,再滴加10mLNaOH溶液,溶液颜色由无色变为红色.可证明为二元酸,用pH计可测定0.05mol﹒L-1H2SO3溶液的PH,若PH大于1,则证明为弱酸.(可提供的仪器:pH计,其他中学化学常见仪器任选,药品:0.10mol﹒L-1NaOH溶液、0.05 mol﹒L-1 H2SO3溶液,酸碱指示剂)
分析 (1)盐酸与亚硫酸钙反应生成氯化钙、二氧化硫与水;
(2)二氧化硫与氢硫酸反应生成硫,反应中二氧化硫表现氧化性;
(3)次氯酸具有强氧化性、二氧化硫具有还原性,不能利用二氧化硫与次氯酸钙直接反应判断亚硫酸与次氯酸的酸性强弱,先验证亚硫酸酸性比碳酸强,再结合碳酸酸性比HClO强碱性判断.A装置制备二氧化硫,由于盐酸易挥发,制备的二氧化硫中混有HCl,用饱和的亚硫酸氢钠除去HCl,再通过碳酸氢钠溶液,可以验证亚硫酸酸性比碳酸强,用酸性高锰酸钾溶液氧化除去二氧化碳中的二氧化硫,用品红溶液检验二氧化碳中二氧化硫是否除尽,再通入F中;
(4)①采取逆流原理通入冷凝水;
②根据关系式:SO2~H2SO4~2NaOH计算;
③残留液中有剩余的盐酸;
(5)用0.10mol﹒L-1NaOH溶液来滴定10mL0.05 mol﹒L-1 H2SO3溶液,消耗NaOH溶液的体积若为10ml证明为二元酸或依据亚硫酸氢钠溶液显酸性,亚硫酸钠溶液显碱性设计实验证明为二元酸,利用测定0.05 mol﹒L-1 H2SO3溶液的PH判断是否完全电离来判断是否为弱酸.
解答 解:(1)盐酸与亚硫酸钙反应生成氯化钙、二氧化硫与水,反应方程式为:CaSO3+2HCl=CaCl2+SO2↑+H2O,
故答案为:CaSO3+2HCl=CaCl2+SO2↑+H2O;
(2)二氧化硫与氢硫酸反应生成硫,反应中二氧化硫表现氧化性,利用装置1中产生的气体证明+4价硫具有氧化性:将SO2通入氢硫酸溶液中,出现淡黄色沉淀,证明+4价硫具有氧化性,
故答案为:将SO2通入氢硫酸溶液溶液中,出现淡黄色沉淀,证明+4价硫具有氧化性;
(3)次氯酸具有强氧化性、二氧化硫具有还原性,不能利用二氧化硫与次氯酸钙直接反应判断亚硫酸与次氯酸的酸性强弱,先验证亚硫酸酸性比碳酸强,再结合碳酸酸性比HClO强碱性判断.A装置制备二氧化硫,由于盐酸易挥发,制备的二氧化硫中混有HCl,用饱和的亚硫酸氢钠除去HCl,再通过碳酸氢钠溶液,可以验证亚硫酸酸性比碳酸强,用酸性高锰酸钾溶液氧化除去二氧化碳中的二氧化硫,用品红溶液检验二氧化碳中二氧化硫是否除尽,再通入F中,则:
装置连接顺序为A、C、B、E、D、F,其中装置C的作用是除去HCl气体,D中品红不褪色,F中出现白色沉淀,可证明亚硫酸的酸性强于次氯酸,
故答案为:A、C、B、E、D、F;除去HCl气体;D中品红不褪色,F中出现白色沉淀;
(4)①采取逆流原理通入冷凝水,即球形冷凝管进水口为b,故答案为:b;
②设残液中SO2含量为xg.L-1,则:
SO2~~H2SO4~~2NaOH
64g 2mol
xg.L-1×0.001L 0.02L×0.1mol/L
所以64g:xg.L-1×0.001L=2mol:0.02L×0.1mol/L
解得x=64.00
故答案为:64.00;
③残留液中有剩余的盐酸,挥发出HCl,会消耗NaOH,导致测定值始终高于实际值,
故答案为:残留液中有剩余的盐酸,导致实验中消耗的氢氧化钠的量偏多;
(5)用0.10mol﹒L-1NaOH溶液来滴定10mL0.05 mol﹒L-1 H2SO3溶液,消耗NaOH溶液的体积为10mL,即证明为二元酸或在滴有酚酞的10mL0.05 mol﹒L-1 H2SO3溶液中,滴加10mL0.10mol﹒L-1NaOH溶液后,先生成的是亚硫酸氢钠溶液显酸性,酚酞颜色不变为无色,再滴加10mLNaOH溶液,和亚硫酸氢钠反应生成亚硫酸钠溶液显碱性酚酞溶液变红色,所以溶液颜色由无色变为红色.可证明为二元酸;用pH计可测定0.05mol﹒L-1 H2SO3溶液的PH,若PH大于1,说嘛氢离子未完全电离出来,溶液中存在电离平衡,则证明为弱酸,
故答案为:用0.10mol﹒L-1NaOH溶液来滴定10mL0.05 mol﹒L-1 H2SO3溶液,消耗NaOH溶液的体积为10mL,即证明为二元酸或在滴有酚酞的10mL0.05 mol﹒L-1 H2SO3溶液中,滴加10mL0.10mol﹒L-1NaOH溶液后,再滴加10mLNaOH溶液,溶液颜色由无色变为红色.可证明为二元酸,用pH计可测定0.05mol﹒L-1 H2SO3溶液的PH,若PH大于1,则证明为弱酸.
点评 本题考查气体制备与性质实验、物质含量测定实验,涉及装置分析与评价、实验方案设计、仪器使用、化学计算等,关键是明确实验原理,较好的考查学生实验综合能力与知识迁移应用,难度中等.

 英才计划期末调研系列答案
英才计划期末调研系列答案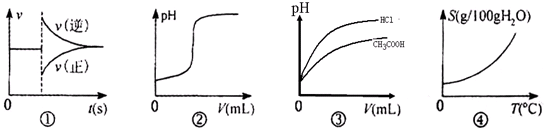
| A. | 图①可以表示对某化学平衡体系改变温度后反应速率随时间的变化 | |
| B. | 图②可以表示向一定量的氢氧化钠溶液中滴加一定浓度的稀硫酸时pH的变化 | |
| C. | 图③可以表示相同pH的醋酸和盐酸溶液分别加水稀释时溶液的pH随体积的变化 | |
| D. | 图④可以表示所有的固体物质溶解度随温度的变化 |
| A. | 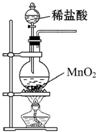 制取少量Cl2 | |
| B. | 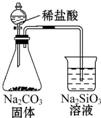 证明非金属性Cl>C>Si | |
| C. | 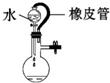 水不能持续流下,说明装置气密性良好 | |
| D. | 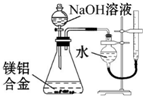 测定镁铝合金中铝的质量分数 |
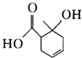
| A. | 能和碳酸钠溶液反应的官能团有2种 | |
| B. | 1mol该有机物最多能与2molH2发生加成 | |
| C. | 与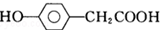 互为同分异构体 互为同分异构体 | |
| D. | 既可以发生取代反应又可以发生氧化反应 |
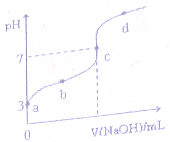 已知常温下CH3COOH的电离平衡常数为 k0,常温下,向20mL 0.1mol•L-1 CH3COOH溶液中逐滴加入0.1mol.L-1NaOH溶液,其 pH变化曲线如图所示(忽略温度变化).下列说法正确的是( )
已知常温下CH3COOH的电离平衡常数为 k0,常温下,向20mL 0.1mol•L-1 CH3COOH溶液中逐滴加入0.1mol.L-1NaOH溶液,其 pH变化曲线如图所示(忽略温度变化).下列说法正确的是( )| A. | a点表溶液中由水电离出的温度为1.0xl0-3mol•L-1 | |
| B. | b 点表示的溶液 c (CH3COO-)<c (Na+) | |
| C. | b、d点表示的溶液中$\frac{c(C{H}_{3}COO)•c({H}^{+})}{c(C{H}_{3}COOH)}$相等 | |
| D. | c点表示CH3COOH和NaOH恰好反应完全 |
| A. | 酒精和水:分液 | |
| B. | 淀粉溶液(胶体)中混有氯化钠:用半透膜进行渗析 | |
| C. | 汽油和柴油:分馏 | |
| D. | 三氯甲烷和水:分液 |
 )和抗癫痫药物H(
)和抗癫痫药物H(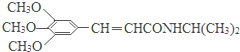 )的路线如图(部分反应略去条件和试剂):
)的路线如图(部分反应略去条件和试剂):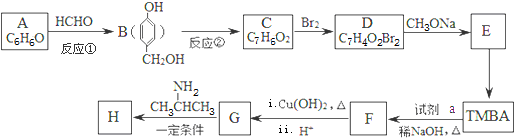
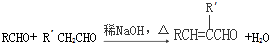 (R、R′表示烃基或氢)
(R、R′表示烃基或氢)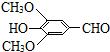 ,试剂a的分子式是C2H4O.
,试剂a的分子式是C2H4O. +2Br2→
+2Br2→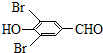 +2HBr.
+2HBr.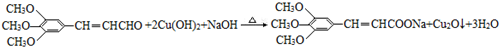 .
.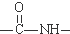 )有类似酯基水解的性质,写出抗癫痫病药物H与足量NaOH溶液发生反应的化学方程式
)有类似酯基水解的性质,写出抗癫痫病药物H与足量NaOH溶液发生反应的化学方程式 +NaOH→
+NaOH→ +H2NCH(CH3)2.
+H2NCH(CH3)2.