题目内容
9.下列物质的分离提纯所用的方法不正确的是( )| A. | 酒精和水:分液 | |
| B. | 淀粉溶液(胶体)中混有氯化钠:用半透膜进行渗析 | |
| C. | 汽油和柴油:分馏 | |
| D. | 三氯甲烷和水:分液 |
分析 A.酒精和水混溶,溶液不分层;
B.淀粉不能透过半透膜;
C.汽油和柴油的沸点不同;
D.三氯甲烷和水互不相溶,溶液分层.
解答 解:A.酒精和水混溶,溶液不分层,应用蒸馏的方法分离,故A错误;
B.淀粉不能透过半透膜,可用渗析的方法分离氯化钠,故B正确;
C.汽油和柴油的沸点不同,可用蒸馏的方法分离,故C正确;
D.三氯甲烷和水互不相溶,溶液分层,可用分液的方法分离,故D正确.
故选A.
点评 本题考查物质的分离、提纯,为高频考点,侧重于物质的性质的考查,注意根据物质的性质的异同选择实验方法,题目难度不大.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
1.在一定的温度下,在恒容容器中可逆反应A(g)+3B(g)?2C(g)达到平衡的标志是B( )
| A. | B生成速率与C分解速率相等 | |
| B. | 容器内气体的平均分子量不再变化 | |
| C. | 单位时间生成n mol A,同时生成3n mol B | |
| D. | 容器内气体的密度不再变化 |
18.${\;}_{1}^{1}$H、${\;}_{1}^{2}$H、${\;}_{1}^{3}$H、H+、H2是( )
| A. | 氢的五种同位素 | B. | 五种氢元素 | ||
| C. | 都不带电荷的粒子 | D. | 氢元素的五种不同粒子 |
 A、B、C、D、E、F、G 原子序数依次增大,A 与 B 不同周期,基态 B 原子核外电子占据 3 个能级,每个能级上电子数相等.D 能形成两种阴离子且电子总数分别为 10、18.E 是短周期电负性最强的元素.基态 F 的价层电子排布式为 ns xnp y,有 n=x+y.基态的+1 价 G 离子核外电子恰好排满三个电子层.
A、B、C、D、E、F、G 原子序数依次增大,A 与 B 不同周期,基态 B 原子核外电子占据 3 个能级,每个能级上电子数相等.D 能形成两种阴离子且电子总数分别为 10、18.E 是短周期电负性最强的元素.基态 F 的价层电子排布式为 ns xnp y,有 n=x+y.基态的+1 价 G 离子核外电子恰好排满三个电子层.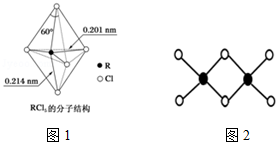 硼及其化合物在工业上有许多用途.工业上以铁硼矿为原料制备硼酸,铁硼矿含有Mg、Fe、Ca、Al、B、O等多种元素,它的主要成分为Mg2B2O5•H2O和Fe3O4.
硼及其化合物在工业上有许多用途.工业上以铁硼矿为原料制备硼酸,铁硼矿含有Mg、Fe、Ca、Al、B、O等多种元素,它的主要成分为Mg2B2O5•H2O和Fe3O4.