题目内容
9.CMU是一种荧光指示剂,可通过下列反应制备: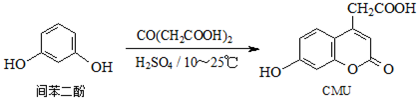
下列说法正确的是( )
| A. | 1molCMU最多可与1molBr2反应 | |
| B. | 1molCMU最多可与3molNaOH反应 | |
| C. | 可用FeCl3溶液鉴别间苯二酚和CMU | |
| D. | CMU在酸性条件下的水解产物只有1种 |
分析 A.CMU中碳碳双键可与溴发生加成反应,酚羟基邻位H原子可被溴取代;
B.CMU中能与氢氧化钠反应的为酚羟基、羧基以及酯基;
C.间苯二酚和CMU都含有酚羟基;
D.CMU含有酯环,水解产物有一种.
解答 解:A.CMU中碳碳双键可与溴发生加成反应,酚羟基邻位H原子可被溴取代,则1molCMU最多可与3molBr2反应,故A错误;
B.CMU中能与氢氧化钠反应的为酚羟基、羧基以及酯基,且酯基可水解生成酚羟基和羧基,则1molCMU最多可与4molNaOH反应,故B错误;
C.间苯二酚和CMU都含有酚羟基,可与氯化铁反应,不能鉴别,故C错误;
D.CMU含有两个环,其中一个为酯环,水解产物有一种,故D正确.
故选D.
点评 本题考查有机物的结构与性质,为高频考点,熟悉有机物中的官能团及物质的性质是解答本题的关键,选项A、B为解答的易错点,题目难度不大.

练习册系列答案
 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案
相关题目
16.室温下.下列指定溶液中微粒的浓度关系正确的是( )
| A. | 0.1mol•L-1NH4Cl溶液中:c(CI-)>c(NH4+)>c(H+)>c(OH-) | |
| B. | 0.1mol•L-1Na2CO3溶液中:c(OH-)=c(H+)+c(HCO3-)+c(H2CO3) | |
| C. | 0.1mol•L-1Na2CO3溶液与同浓度等体积盐酸混合的溶液中:c(Na+)>c(CI-)>c(CO32-)>c(HCO3-) | |
| D. | 0.2mol•L-1H2C2O4(弱酸)与0.1mol•L-1NaOH溶液等体积混合的溶液中:2[c(H+)-c(OH-)]=3c(C2O42-)-c(H2C2O4)+c(HC2O4-) |
20.NH2OH(羟胺)是有机合成中常用的还原剂,是一元弱碱.25℃时,其电离平衡常数Kb=9.1×10-9.下列有关叙述错误的是( )
| A. | 羟胺中氮显-1价 | |
| B. | 羟胺的电子式为 | |
| C. | 硫酸羟胺的化学式为(NH3OH)2SO4 | |
| D. | 羟胺的电离方程式为NH2OH?NH2O-+H+ |
17.下列化学反应的离子方程式正确的是( )
| A. | 氯气与溴化钾溶液反应:Cl2+2Br-=2Cl-+Br2 | |
| B. | 铜片插人硝酸银溶液中:Cu+Ag+=Cu2++Ag | |
| C. | 单质铁与稀盐酸反应:2Fe+6H+=2Fe3++3H2↑ | |
| D. | 碳酸钠溶液与醋酸反应:CO32-+2H+=CO2↑+H2O |
4.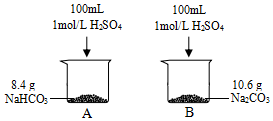 某小组同学在实验室研究Na2CO3与NaHCO3的性质.
某小组同学在实验室研究Na2CO3与NaHCO3的性质.
实验Ⅰ:
(1)产生气体的速率A> B(填“>”或“<”或“=”),结合化学用语说明原因Na2CO3与酸反应经历两步:CO32-+H+=HCO3-HCO3-+H+=H2O+CO2↑,而NaHCO3只有一步,因此A中产生气体速率更快.
(2)产生气体的体积A= B(填“>”或“<”或“=”),标准状况下,A烧杯中产生气体的体积为2.24L
(3)任意写出一种将NaHCO3转变为Na2CO3的方法2NaHCO3 $\frac{\underline{\;加热\;}}{\;}$Na2CO3+H2O+CO2↑(用化学方程式表示).
实验Ⅱ:1mL 0.1mol/L NaHCO3溶液与1mL 0.01mol/L Ca(OH)2溶液混合产生CaCO3白色沉淀.
(4)请用离子方程式表示生成CaCO3的反应过程HCO3-+OH-=CO32-+H2O,Ca2++CO32-=CaCO3↓.
(5)同学们设计了如下实验方案,验证上述反应过程,请将方案补充完整:
 某小组同学在实验室研究Na2CO3与NaHCO3的性质.
某小组同学在实验室研究Na2CO3与NaHCO3的性质.实验Ⅰ:
(1)产生气体的速率A> B(填“>”或“<”或“=”),结合化学用语说明原因Na2CO3与酸反应经历两步:CO32-+H+=HCO3-HCO3-+H+=H2O+CO2↑,而NaHCO3只有一步,因此A中产生气体速率更快.
(2)产生气体的体积A= B(填“>”或“<”或“=”),标准状况下,A烧杯中产生气体的体积为2.24L
(3)任意写出一种将NaHCO3转变为Na2CO3的方法2NaHCO3 $\frac{\underline{\;加热\;}}{\;}$Na2CO3+H2O+CO2↑(用化学方程式表示).
实验Ⅱ:1mL 0.1mol/L NaHCO3溶液与1mL 0.01mol/L Ca(OH)2溶液混合产生CaCO3白色沉淀.
(4)请用离子方程式表示生成CaCO3的反应过程HCO3-+OH-=CO32-+H2O,Ca2++CO32-=CaCO3↓.
(5)同学们设计了如下实验方案,验证上述反应过程,请将方案补充完整:
| 实验步骤 | 实验现象 |
| ⅰ.取1mL 0.1mol/L NaHCO3溶液,向其中加入 1mL 0.01mol/L CaCl2溶液 | 无明显现象 |
| ⅱ.向上述溶液中滴加NaOH溶液 | 产生白色沉淀 |
2.某温度下,在固定容积的密闭容器中,可逆反应A(g)+3B(g)?2C(g)达到平衡时,各物质的物质的量之比为n(A):n(B):n(C)=2:2:1.保持温度不变,以2:2:1的物质的量之比再充入A、B、C,则( )
| A. | 平衡正向移动 | |
| B. | 再达平衡时,n(A):n(B):n(C)仍为2:2:1 | |
| C. | 再达平衡时,C的体积分数减小 | |
| D. | 再达平衡时,正反应速率增大,逆反应速率减小 |
9.下列说法不正确的是( )
| A. | 氯气可用于漂白纸浆 | |
| B. | 热的纯碱溶液可以去除物品表面的油污 | |
| C. | 钠钾合金常温下是液体,可用于快中子反应堆的热交换剂 | |
| D. | 浓硫酸的吸水性,可使蔗糖炭化,实验室常用作干燥剂 |
7.下列浓度关系正确的是( )
| A. | Na2CO3溶液中:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+) | |
| B. | 氯水中:c(Cl-)>c(H+)>c(OH-)>c(ClO-) | |
| C. | 等体积等浓度的氢氧化钠与醋酸混合:c(Na+)=c(CH3COO-) | |
| D. | 氯水中:c(Cl2)=2[c(ClO-)+c(Cl-)+c(HClO)] |