题目内容
20.NH2OH(羟胺)是有机合成中常用的还原剂,是一元弱碱.25℃时,其电离平衡常数Kb=9.1×10-9.下列有关叙述错误的是( )| A. | 羟胺中氮显-1价 | |
| B. | 羟胺的电子式为 | |
| C. | 硫酸羟胺的化学式为(NH3OH)2SO4 | |
| D. | 羟胺的电离方程式为NH2OH?NH2O-+H+ |
分析 A、NH2OH(羟胺)中H元素为+1价,O元素为-2价,根据化合价代数和为0来分析;
B、NH2OH为共价化合物;
C、NH2OH为一元弱碱,在和硫酸反应时生成硫酸羟胺;
D、NH2OH是一元弱碱.
解答 解:A、NH2OH(羟胺)中H元素为+1价,O元素为-2价,根据化合价代数和为0可知,其中N元素的价态为-1价,故A正确;
B、NH2OH为共价化合物,由-NH2和-OH构成,即N原子分别和两个H原子、一个O原子形成共价键,故电子式为 ,故B正确;
,故B正确;
C、NH2OH为一元弱碱,在和硫酸反应时生成硫酸羟胺,化学式为(NH3OH)2SO4,故C正确;
D、NH2OH是一元弱碱,故电离方程式为NH2OH?NH2++OH-,故D错误.
故选D.
点评 本题借助学生对一水合氨性质的掌握考查了一种陌生的化合物--NH2OH的有关性质,应注意知识的迁移运用,难度不大,

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
7.雷雨天气中,发生自然固氮的氮元素在土壤中的主要存在形式是( )
| A. | NH4+ | B. | NO3- | C. | HNO3 | D. | NH3•H2O |
11.下列说法正确的是( )
| A. | 为了使婴儿对食品有更浓厚的兴趣,应在婴儿食品中加入大量的着色剂 | |
| B. | 为了使火腿肠颜色更鲜红,可多加入一些亚硝酸钠 | |
| C. | 蛋白质在人体内经消化后生成碳酸、硫酸、尿酸等,故属于酸性食物 | |
| D. | 常用的抗酸药有氢氧化铜、氢氧化铝、柠檬酸钠、碳酸钙等 |
8.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 含有NA个氦原子的氦气的物质的量为2摩尔 | |
| B. | 2摩尔水的摩尔质量是1摩尔水的摩尔质量的2倍 | |
| C. | 25℃,1.01×105Pa,64g的SO2中含有的原子数为3NA | |
| D. | l摩尔任何物质所含的分子数均为NA |
15.下列各组反应中,不能用同一个离子方程式表示的是( )
| A. | 盐酸分别与氢氧化钠溶液、澄清石灰水反应 | |
| B. | 硫酸分别与氢氧化钠溶液、氢氧化钡溶液反应 | |
| C. | 硝酸分别与碳酸钠溶液、碳酸钾溶液反应 | |
| D. | 锌分别与稀盐酸、稀硫酸反应 |
5.用NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 密闭容器中,0.5molN2与1.5molH2充分反应后所得的氨分子数为NA | |
| B. | 25℃时,1LpH=13的Ba(OH)2溶液中含有的OH-数目为0.2NA | |
| C. | 46g由Na2O2和N2O4组成的混合气体中含有的氧原子数为NA | |
| D. | 含2molH2SO4的浓硫酸与足量铜共热,转移的电子数为2NA |
12.实验室配制250mL 0.1mol•L-1Na2CO3溶液时,不需要用到的仪器是( )
| A. | 容量瓶 | B. | 烧杯 | C. | 玻璃棒 | D. | 酒精灯 |
9.CMU是一种荧光指示剂,可通过下列反应制备:
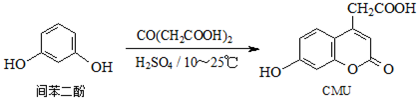
下列说法正确的是( )
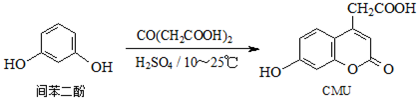
下列说法正确的是( )
| A. | 1molCMU最多可与1molBr2反应 | |
| B. | 1molCMU最多可与3molNaOH反应 | |
| C. | 可用FeCl3溶液鉴别间苯二酚和CMU | |
| D. | CMU在酸性条件下的水解产物只有1种 |
18.下列物质属于烃类的是( )
| A. | C2H5OH | B. | C3H8 | C. | CH3Br | D. | C6H5NO2 |