题目内容
2.下列7种固态物质:A.P4、B.SiO2、C.NH4Cl、D.Ca(OH)2、E.NaF、F.CO2(干冰)、G.金刚石,将正确的序号(字母)填入下列空中.(1)既有离子键又有共价键的是CD.
(2)熔化时不需要破坏化学键的是AF,熔化时需要破坏共价键的是BG.
分析 (1)活泼金属与活泼非金属之间形成离子键,非金属之间形成共价键;
(2)离子晶体熔化时破坏离子键;原子晶体熔化时破坏共价键;分子晶体破坏分子间作用力.
解答 解:(1)活泼金属与活泼非金属之间形成离子键,铵根离子与阴离子之间形成离子键,非金属之间形成共价键,则晶体中既有离子键又有共价键的是NH4Cl、Ca(OH)2;
故答案为:CD;
(2)P4、CO2属于分子晶体,熔化时破坏分子间作用力,不会破坏化学键;SiO2、金刚石属于原子晶体,熔化时破坏共价键;
故答案为:AF;BG.
点评 本题考查的知识点较多,侧重考查学生对离子键、共价键,离子化合物、共价化合物的辨别能力,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
13.某同学按下列步骤配制500mL 0.20mol•L-1NaOH溶液,请回答有关问题.
| 实验步骤 | 有关问题 |
| (1)计算所需NaOH的质量 | 需要NaOH的质量为4.0g |
| (2)称量NaOH固体 | 称量过程中主要用到的仪器是 托盘天平、药匙 |
| (3)将NaOH加入100mL烧杯中,加适量蒸馏水溶解 | 为加快溶解,可采取的措施是 搅拌、加热、研细氢氧化钠等措施 |
| (4)将烧杯中的溶液转移至500mL容量瓶中 | 为防止溶液溅出,应该采取的措施是 玻璃棒引流 |
| (5)向容量瓶中加蒸馏水至刻度线 | 在进行此操作时应注意的问题是 加水至液面距离刻度线1~2cm时,改用胶头滴管滴加至溶液凹液面与刻度线水平相切 |
10.配置一定体积、一定物质的量的浓度的Na2CO3溶液时,下列情况可能使溶液浓度偏低的是( )
| A. | 容量瓶内有少量蒸馏水 | |
| B. | 溶液从烧杯中转移到容量瓶时,没有洗涤烧杯 | |
| C. | 定容时观察液面时俯视定容 | |
| D. | 配溶液的Na2CO3•10H2O晶体在空气中久置风化 |
17.短周期元素X、Y、Z在周期表中的位置如表所示,则下列说法正确的是( )
| X | ||
| Y | ||
| Z |
| A. | Z一定是活泼的金属 | |
| B. | Y的最高化合价为+7价 | |
| C. | Z的最高价氧化物的水化物是强酸 | |
| D. | 1molY单质与足量水反应时,有2mol电子发生转移 |
7.在有机物分子中,若某个碳原子连接4个不同的原子或原子团,则将这种碳原子称为“手性碳原子”.凡有一个手性碳原子的物质一定具有光学活性.物质有光学活性,它发生下列反应后生成的有机物仍有光学活性的是( )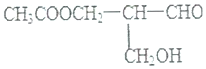
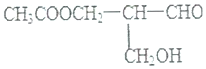
| A. | 与NaOH溶液共热 | B. | 与甲酸发生酯化反应 | ||
| C. | 与碱性Cu(OH)2悬浊液反应 | D. | 在催化剂存在下与H2作用 |
14.下列有关化学键的叙述,正确的是( )
| A. | 单质分子均不存在化学键 | |
| B. | 共价化合物中一定含有共价键,也可能含有离子键 | |
| C. | 含有共价键的化合物一定是共价化合物 | |
| D. | 离子化合物中一定含有离子键,也可能含有共价键 |
12.原子序数依次增大的元素a、b、c、d,它们的最外层电子数分别为1、6、7、1.a-的电子层结构与氦相同,b和c的次外层有8个电子,c-和d+的电子层结构相同.下列叙述错误的是( )
| A. | 氧化物对应的水化物的酸性:b<c | |
| B. | 元素的非金属性次序为:c>b>a | |
| C. | d与其他3种元素均能形成离子化合物 | |
| D. | 含d元素的化合物的焰色反应呈紫色 |