题目内容
6.下列各组元素性质的递变情况错误的是( )| A. | Li、Be、B原子最外层电子数依次增多 | |
| B. | P、S、Cl元素最高正价依次升高 | |
| C. | N、O、F原子得电子能力减弱 | |
| D. | Na、K、Rb的电子层数逐渐增多 |
分析 A.同周期从左向右最外层电子数增多;
B.第三周期从左向右元素最高正价增大;
C.同周期从左向右得电子能力增强;
D.同主族从上到下电子层增多.
解答 解:A.同周期从左向右最外层电子数增多,则Li、Be、B原子最外层电子数依次增多,故A正确;
B.第三周期从左向右元素最高正价增大,则P、S、Cl元素最高正价依次升高,故B正确;
C.同周期从左向右得电子能力增强,则N、O、F原子得电子能力依次增强,故C错误;
D.同主族从上到下电子层增多,则Na、K、Rb的电子层数逐渐增多,故D正确;
故选C.
点评 本题考查元素周期表和周期律,为高频考点,把握元素的位置、性质及元素周期律为解答的关键,侧重分析与应用能力的考查,注重基础知识的夯实和训练,题目难度不大.

练习册系列答案
相关题目
14.下列物质属于电解质的是( )
| A. | 蔗糖 | B. | 玻璃 | C. | 纯碱 | D. | 铁 |
15.乳酸的结构简式如图,对乳酸的化学性质推测不正确的是( )
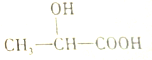
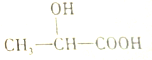
| A. | 1mol乳酸可以与足量的NaHCO3反应生成1molCO2 | |
| B. | 1mol乳酸可以与足量的钠反应生成1mol氢气 | |
| C. | 乳酸可以在一定条件下发生消去反应生成CH2=CHCOOH | |
| D. | 乳酸可以与NaOH溶液反应生成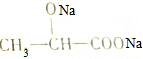 |
14.酸性KMnO4溶液能与草酸(H2C2O4)溶液反应.某探究小组利用反应过程中溶液紫色消失快慢的方法来研究影响反应速率的因素.
Ⅰ.实验前首先用浓度为0.1000mol•L-1酸性KMnO4标准溶液滴定未知浓度的草酸.
(1)写出滴定过程中发生反应的化学方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O.
(2)滴定过程中操作滴定管的图1示正确的是A.
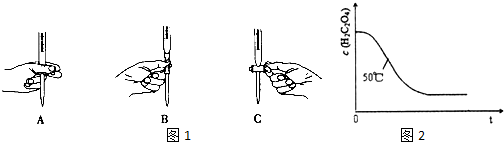
(3)若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的草酸溶液浓度偏高(填“偏高”、“偏低”、或“不变”).
Ⅱ.通过滴定实验得到草酸溶液的浓度为0.2000mol•L-1.用该草酸溶液按下表进行后续实验(每次实验草酸溶液的用量均为8mL).
(4)写出表中a 对应的实验目的探究温度不同对反应速率的影响;若50℃时,草酸浓度c(H2C2O4)随反应时间t的变化曲线如图2所示,保持其他条件不变,请在图中画出25℃时c(H2C2O4)随t的变化曲线示意图.
(5)该小组同学对实验1和3分别进行了三次实验,测得以下实验数据(从混合振荡均匀开始计时):
分析上述数据后得出“当其它条件相同时,酸性高锰酸钾溶液的浓度越小,褪色时间就越短,即反应速率就越快”的结论.甲同学认为该小组“探究反应物浓度对速率影响”的实验方案设计中存在问题,从而得到了错误的实验结论,请简述甲同学改进的实验方案其它条件相同时,利用等量且少量的高锰酸钾与等体积不同浓度的足量草酸溶液反应,测量溶液褪色时间.
(6)该实验中使用的催化剂应选择MnSO4而不是MnCl2,原因可用离子方程式表示为2MnO4-+10Cl-+16H+=5Cl2↑+2Mn2++8H2O.
Ⅰ.实验前首先用浓度为0.1000mol•L-1酸性KMnO4标准溶液滴定未知浓度的草酸.
(1)写出滴定过程中发生反应的化学方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O.
(2)滴定过程中操作滴定管的图1示正确的是A.

(3)若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的草酸溶液浓度偏高(填“偏高”、“偏低”、或“不变”).
Ⅱ.通过滴定实验得到草酸溶液的浓度为0.2000mol•L-1.用该草酸溶液按下表进行后续实验(每次实验草酸溶液的用量均为8mL).
| 实验编号 | 温度(℃) | 催化剂 用量(g) | 酸性高锰酸钾溶液 | 实验目的 a.实验1和2探究探究温度不同对反应速率的影响; b.实验1和3探究反应物浓度对该反应速率的影响; c.实验1和4探究催化剂对该反应速率的影响. | |
| 体积 (mL) | 浓度 (mol•L-1) | ||||
| 1 | 25 | 0.5 | 4 | 0.1000 | |
| 2 | 50 | 0.5 | 4 | 0.1000 | |
| 3 | 25 | 0.5 | 4 | 0.0100 | |
| 4 | 25 | 0 | 4 | 0.1000 | |
(5)该小组同学对实验1和3分别进行了三次实验,测得以下实验数据(从混合振荡均匀开始计时):
| 实验编号 | 溶液褪色所需时间(min) | ||
| 第1次 | 第2次 | 第3次 | |
| 1 | 14.0 | 13.0 | 11.0 |
| 3 | 6.5 | 6.7 | 6.8 |
(6)该实验中使用的催化剂应选择MnSO4而不是MnCl2,原因可用离子方程式表示为2MnO4-+10Cl-+16H+=5Cl2↑+2Mn2++8H2O.
1.表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:(无特殊说明均填元素符号、化学式等化学用语)
(1)在这些元素中,化学性质最不活泼的是Ne,元素原子半径最小的是H,被称为“国防金属”的是Mg,被称为“生命元素”的是P,单质氧化性最强的元素是F.
(2)元素②的一种同位素(含8个中子)可测定文物年代,这种同位素的符号是${\;}_{6}^{14}$C.
(3)在上述元素的最高价氧化物对应水化物中,碱性最强的化合物的化学式是KOH.酸性最强的化合物的化学式是HClO4.
(4)写出③的气态氢化物与其最高价氧化物对应水化物反应的方程式NH3+HNO3=NH4NO3.
(5)元素④的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑.
| 主族 周期 | IA | ⅡA | IIIA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ⑥ | |||
| 3 | ⑦ | ⑧ | ⑨ | |||||
| 4 | ⑩ |
(2)元素②的一种同位素(含8个中子)可测定文物年代,这种同位素的符号是${\;}_{6}^{14}$C.
(3)在上述元素的最高价氧化物对应水化物中,碱性最强的化合物的化学式是KOH.酸性最强的化合物的化学式是HClO4.
(4)写出③的气态氢化物与其最高价氧化物对应水化物反应的方程式NH3+HNO3=NH4NO3.
(5)元素④的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑.
11.pH与体积均相同的氢氧化钠溶液和氨水,分别与同浓度、同体积的AlCl3溶液反应,生成沉淀的质量也相同,则可能是( )
| A. | AlCl3过量 | |
| B. | AlCl3的量恰好与氢氧化钠完全反应 | |
| C. | 两种碱均过量 | |
| D. | AlCl3的量恰好与氨水完全反应 |
18.下列描述中,不符合生产实际的是( )
| A. | 电解熔融的氯化钠可制取金属钠,电解熔融的氧化铝可制取金属铝 | |
| B. | 电解精炼铜时,同一时间内阳极溶解铜的质量比阴极析出铜的质量小 | |
| C. | 在镀件上电镀锌,用锌作阳极,镀件作阴极 | |
| D. | 电解法精炼粗铜,用纯铜作阳极,粗铜阴极,CuSO4溶液为电解液 |
16.在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)?2Z(g);△H<0,一段时间后达到平衡.反应过程中测定的数据如下表:
下列说法正确的是( )
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A. | 0~2 min的平均速率v(Z)=2.0×10-3 mol•L-1•min-1 | |
| B. | 其他条件不变,降低温度,反应达到新平衡前 v(正)<v(逆) | |
| C. | 该温度下此反应的平衡常数K=144 | |
| D. | 其他条件不变,再充入0.2 mol Z,平衡时X的体积分数不变 |

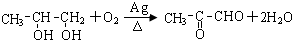 .
.