题目内容
下列化学用语书写正确的是( )
A、氯原子的结构示意图: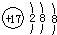 | ||
B、作为相对原子质量测定标准的碳核素:
| ||
C、氯化镁的电子式: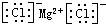 | ||
| D、乙烯的结构简式:CH2CH2 |
考点:电子式、化学式或化学符号及名称的综合,原子结构示意图,结构简式
专题:
分析:A.氯原子的核电荷数、核外电子数都是17, 为氯离子结构示意图;
为氯离子结构示意图;
B.作为相对原子质量测定标准的碳核素为:碳-12,质量数为12;
C.氯化镁为离子化合物,其电子式需要标出离子所带电荷,氯离子子需要标出最外层核外电子数;
D.乙烯的官能团为碳碳双键,结构简式中需要标出官能团.
 为氯离子结构示意图;
为氯离子结构示意图;B.作为相对原子质量测定标准的碳核素为:碳-12,质量数为12;
C.氯化镁为离子化合物,其电子式需要标出离子所带电荷,氯离子子需要标出最外层核外电子数;
D.乙烯的官能团为碳碳双键,结构简式中需要标出官能团.
解答:
解:A.氯离子的核外电子数为17,氯离子的原子结构示意图为: ,故A错误;
,故A错误;
B.作为相对原子质量测定标准的碳核素为C-12,其正确的表示方法为:612C,故B错误;
C.氯化镁中存在阴阳离子,氯化镁的电子式为: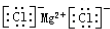 ,故C正确;
,故C正确;
D.乙烯分子中含有碳碳双键,乙烯正确的结构简式为:CH2═CH2,故D错误;
故选C.
 ,故A错误;
,故A错误;B.作为相对原子质量测定标准的碳核素为C-12,其正确的表示方法为:612C,故B错误;
C.氯化镁中存在阴阳离子,氯化镁的电子式为:
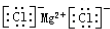 ,故C正确;
,故C正确;D.乙烯分子中含有碳碳双键,乙烯正确的结构简式为:CH2═CH2,故D错误;
故选C.
点评:本题考查了常见化学用语的判断,题目难度中等,注意掌握原子结构示意图、电子式、结构简式的概念及表示方法,明确电子式、分子式、结构简式、结构式及原子结构示意图与离子结构示意图的区别,试题培养了学生规范答题的能力.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
下列物质是生活中常见的物质,属于强电解质的是( )
| A、干冰 |
| B、BaSO4 |
| C、醋酸 |
| D、酒精 |
25℃时,某强酸溶液pH=a,强碱溶液pH=b,且a+b=13,酸碱溶液混合后溶液的pH=7,则酸溶液的体积(V1)与碱溶液的体积(V2)的关系是( )
| A、V1=10V2 |
| B、V1=2V2 |
| C、V2=10V1 |
| D、V2=2 V1 |
某元素原子的最外电子层上只有2个电子,该元素是( )
| A、一定是ⅡA元素 |
| B、一定是金属元素 |
| C、可能是金属元素也可能是非金属元素 |
| D、该元素为正二价 |
已知:CH4(g)+2O2(g)→CO2(g)+2H2O(l)+890kJ、CO(g)+
O2(g)→CO2(g)+282.5kJ.标准情况下,由CH4、CO、CO2组成的混合气体89.6L完全燃烧时能放出1010kJ的热量,并生成18g液体水,则燃烧前混合气体中CO占的体积分数为( )
| 1 |
| 2 |
| A、50% | B、60% |
| C、70% | D、80% |
NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、2.8 g乙烯和丙烯的混合物中所含碳原子数为0.2NA |
| B、4.48 L H2和O2的混合物中所含分子数为0.2NA |
| C、4 g重水(D2O)中所含质子数为0.2NA |
| D、200 mL 1 mol/L的氨水中含NH3?H2O分子数为0.2NA |
下列水解离子方程式正确的是( )
| A、CH3COO-+H2O?CH3COOH+OH- |
| B、NH4++H2O?NH4OH+H+ |
| C、Fe3++H2O?Fe(OH)3+H+ |
| D、Al3++3HCO3-═Al(OH)3↓+3CO2↑ |


 反应制得有机物B(分子式为C9H8O4,遇FeCl3溶液不能显色),该反应的化学方程式是
反应制得有机物B(分子式为C9H8O4,遇FeCl3溶液不能显色),该反应的化学方程式是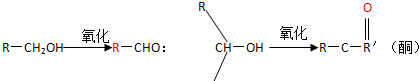
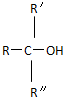 则很难被氧化(R、R+、R表示羟基).
则很难被氧化(R、R+、R表示羟基).