题目内容
下列水解离子方程式正确的是( )
| A、CH3COO-+H2O?CH3COOH+OH- |
| B、NH4++H2O?NH4OH+H+ |
| C、Fe3++H2O?Fe(OH)3+H+ |
| D、Al3++3HCO3-═Al(OH)3↓+3CO2↑ |
考点:离子方程式的书写
专题:
分析:A.醋酸根为弱酸根离子水解生成醋酸与氢氧根离子;
B.铵根离子为弱碱阳离子水解生成一水合氨和氢离子;
C.电荷不守恒;
D.铝离子与碳酸氢根离子发生双水解生成氢氧化铝沉淀和二氧化碳气体.
B.铵根离子为弱碱阳离子水解生成一水合氨和氢离子;
C.电荷不守恒;
D.铝离子与碳酸氢根离子发生双水解生成氢氧化铝沉淀和二氧化碳气体.
解答:
解:A.醋酸根离子水解的离子方程式为:CH3COO-+H2O?CH3COOH+OH-,故A正确;
B.氨根离子水解的离子方程式为:NH4++H2O?NH3?H2O+H+,故B错误;
C.三价铁离子水解的离子方程式为:Fe3++3H2O?Fe(OH)3+3H+,故C错误;
D.铝离子与碳酸氢根离子发生双水解生成氢氧化铝沉淀和二氧化碳气体,离子方程式为:Al3++3HCO3-═Al(OH)3↓+3CO2↑,故D正确;
故选:AD.
B.氨根离子水解的离子方程式为:NH4++H2O?NH3?H2O+H+,故B错误;
C.三价铁离子水解的离子方程式为:Fe3++3H2O?Fe(OH)3+3H+,故C错误;
D.铝离子与碳酸氢根离子发生双水解生成氢氧化铝沉淀和二氧化碳气体,离子方程式为:Al3++3HCO3-═Al(OH)3↓+3CO2↑,故D正确;
故选:AD.
点评:本题考查了离子方程式的书写,侧重考查水解离子方程式,明确离子的性质和水解的规律是解题关键,注意双水解彻底,用等号,标注气体符号、沉淀符号.

练习册系列答案
相关题目
为了验证NaHCO3固体中是否含有Na2CO3,下列实验及判断中,正确的是( )
| A、加热,观察是否有气体放出 |
| B、溶于水后加BaC12,看有无沉淀 |
| C、溶于水后加石灰水,看有无沉淀 |
| D、取固体变色试样加盐酸,看是否有气泡产生 |
实验室用足量镁粉与一定量的某浓度的盐酸反应来制得氢气.由于反应速率太快,不易操作.为减慢反应速率,同时又不影响生成H2的总量,可向盐酸中加入的物质是( )
| A、CH3COONa固体 |
| B、NaOH溶液 |
| C、(NH4)2SO4粉末 |
| D、K2SO4固体 |
下列化学用语书写正确的是( )
A、氯原子的结构示意图: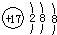 | ||
B、作为相对原子质量测定标准的碳核素:
| ||
C、氯化镁的电子式: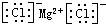 | ||
| D、乙烯的结构简式:CH2CH2 |
阿伏加德罗常数约为6.02×1023mol-1,下列说法中一定正确的是( )
| A、常温常压下,22g氧气和26g臭氧混合气体所含氧原子总数为3×6.02×1023 |
| B、1L0.5mol/L的CH3COONa溶液中含有的CH3COO-数为0.5×6.02×1023 |
| C、常温常压下,16g14CH4所含中子数为8×6.02×1023 |
| D、1molCl2发生反应时,转移的电子数一定是2NA |
下列化学用语的表示,不正确的是( )
A、NaCl的电子式: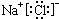 |
B、Mg原子结构示意图: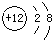 |
| C、乙烯的结构简式:CH2=CH2 |
D、甲烷的结构式: |

 铝镁合金已成为轮船制造、化工生产等行业的重要材料.研究性学习小组的同学,为测定某不同品牌铝镁合金(不含其它元素)中镁的质量分数,设计下列两种不同实验方案进行探究.填写下列空白.
铝镁合金已成为轮船制造、化工生产等行业的重要材料.研究性学习小组的同学,为测定某不同品牌铝镁合金(不含其它元素)中镁的质量分数,设计下列两种不同实验方案进行探究.填写下列空白.