题目内容
某元素原子的最外电子层上只有2个电子,该元素是( )
| A、一定是ⅡA元素 |
| B、一定是金属元素 |
| C、可能是金属元素也可能是非金属元素 |
| D、该元素为正二价 |
考点:元素周期表的结构及其应用
专题:元素周期律与元素周期表专题
分析:元素周期中,原子最外电子层只有2个电子的元素,为He、碱土金属(ⅡA)或某些过渡金属元素,以此来解答.
解答:
解:元素周期中,原子最外电子层只有2个电子的元素,为He、碱土金属(ⅡA)或某些过渡金属元素,可能为金属元素,也可能为非金属元素,还可能为可能是稀有气体元素,可能易失去电子,也可能不易失去电子,若为He,不存在+2价,
故选C.
故选C.
点评:本题考查元素周期表的结构及应用,为高频考点,把握最外层电子数为2的元素及位置与原子结构的关系为解答的关键,注意常见元素的位置及可能元素分析,题目难度不大.

练习册系列答案
 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
下表列出了25℃时有关弱酸的电离平衡常数:则有关说法正确的是( )
| 弱酸 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×10-5 | 4.9×l0-1 | K1=4.3×10-7 K2=5.6×10-11 |
| A、等物质的量浓度的各溶液pH关系为:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa) |
| B、95℃纯水的pH<7,说明加热可导致水呈酸性 |
| C、pH=3的醋酸溶液,稀释至10倍后pH=4 |
| D、0.02mol/L的盐酸,与等体积水混合后pH=2 |
把0.05mol NaOH固体分别加入下列100mL液体中,溶液导电能力变化不大的是( )
| A、自来水 |
| B、0.5mol/L盐酸 |
| C、0.5mol/LCH3COOH |
| D、0.5mol/LNH4Cl溶液 |
实验室用足量镁粉与一定量的某浓度的盐酸反应来制得氢气.由于反应速率太快,不易操作.为减慢反应速率,同时又不影响生成H2的总量,可向盐酸中加入的物质是( )
| A、CH3COONa固体 |
| B、NaOH溶液 |
| C、(NH4)2SO4粉末 |
| D、K2SO4固体 |
已知下列热化学方程式:2Zn(s)+O2(g)=2ZnO(s);△H1=-702.2kJ/mol
2Hg(l)+O2(g)=2HgO(s);△H2=-181.4kJ/mol
由此可知热化学方程式Zn(s)+HgO(s)=ZnO(s)+Hg(l)的反应热△H3为( )
2Hg(l)+O2(g)=2HgO(s);△H2=-181.4kJ/mol
由此可知热化学方程式Zn(s)+HgO(s)=ZnO(s)+Hg(l)的反应热△H3为( )
| A、-441.8kJ/mol |
| B、-520.8kJ/mol |
| C、-883.6kJ/mol |
| D、-260.4kJ/mol |
下列化学用语书写正确的是( )
A、氯原子的结构示意图: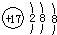 | ||
B、作为相对原子质量测定标准的碳核素:
| ||
C、氯化镁的电子式: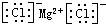 | ||
| D、乙烯的结构简式:CH2CH2 |
下列化学用语的表示,不正确的是( )
A、NaCl的电子式: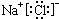 |
B、Mg原子结构示意图: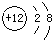 |
| C、乙烯的结构简式:CH2=CH2 |
D、甲烷的结构式: |

