题目内容
14.12mL浓度为0.10mol•L-1的Na2SO3溶液,恰好与10mL浓度为0.04mol?L-1的K2Cr2O7溶液完全反应,已知Na2SO3能被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为( )| A. | +5 | B. | +4 | C. | +3 | D. | +2 |
分析 n(Na2SO3)=0.1mol/L×0.012L=0.0012mol,n(K2Cr2O7)=0.04mol/L×0.01L=0.0004mol,亚硫酸钠具有还原性,所以在反应中被氧化生成硫酸钠,K2Cr2O7具有氧化性,所以在反应中得电子发生还原反应,再根据氧化还原反应中得失电子相等进行计算.
解答 解:n(Na2SO3)=0.1mol/L×0.012L=0.0012mol,n(K2Cr2O7)=0.04mol/L×0.01L=0.0004mol,亚硫酸钠具有还原性,所以在反应中被氧化生成硫酸钠,
K2Cr2O7具有氧化性,所以在反应中得电子发生还原反应,
设元素Cr在还原产物中的化合价是x,根据得失电子相等,则
0.0012mol×(6-4)=0.0004mol×2×(6-x),
3=(6-x),所以x=+3,
故选C.
点评 本题考查了氧化还原反应的有关计算,为高频考点,侧重于学生的分析能力和计算能力的考查,根据氧化还原反应中得失电子相等进行解答即可,难度不大.

练习册系列答案
相关题目
4.下列叙述正确的是( )
| A. | 锅炉水垢中的CaSO4经饱和碳酸钠溶液浸泡可转化为CaCO3 | |
| B. | 常温下,在含有Ag+和Cl-的溶液中,Ag+和Cl-浓度之积是个常数 | |
| C. | 当醋酸达到电离平衡后,改变某条件电离平衡向正反应方向移动,则溶液的导电能力一定变强 | |
| D. | 将浓度为0.1 mol/L的HF溶液加水不断稀释,溶液$\frac{c({F}^{-})}{c({H}^{+})}$始终保持增大 |
5.向一体积不变的密闭容器中加入2mol A、0.6mol C和一定量的B三种气体.一定条件下发生反应,各物质浓度随时间变化如图一所示.图二为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件.已知t3~t4阶段使用了催化剂;图一中t0~t1阶段c(B)未画出.
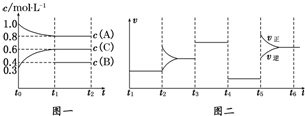
(1)若t1=15min,则t0~t1阶段以C浓度变化表示的反应速率为v(C)=0.02 mol/(L•min).
(2)t4~t5阶段改变的条件为减小压强,B的起始物质的量为1.0 mol.各阶段平衡时对应的平衡常数如下表所示:
则K1=0.84(保留两位小数),K1、K2、K3、K4、K5之间的关系为K1=K2=K3=K4<K5(用“>”、“<”或“=”连接).
(3)t5~t6阶段保持容器内温度不变,若A的物质的量共变化了0.01mol,而此过程中容器与外界的热交换总量为a kJ,写出此温度下该反应的热化学方程式:2A(g)+B(g)?3C(g)△H=+200a kJ/mol.
(4)在相同条件下,若起始时容器中加入a mol A、b mol B和c mol C,要达到t1时刻同样的平衡,a、b、c要满足的条件为a+$\frac{2}{3}$c=2.4,b+$\frac{1}{3}$c=1.2.

(1)若t1=15min,则t0~t1阶段以C浓度变化表示的反应速率为v(C)=0.02 mol/(L•min).
(2)t4~t5阶段改变的条件为减小压强,B的起始物质的量为1.0 mol.各阶段平衡时对应的平衡常数如下表所示:
| t1~t2 | t2~t3 | t3~t4 | t4~t5 | t5~t6 |
| K1 | K2 | K3 | K4 | K5 |
(3)t5~t6阶段保持容器内温度不变,若A的物质的量共变化了0.01mol,而此过程中容器与外界的热交换总量为a kJ,写出此温度下该反应的热化学方程式:2A(g)+B(g)?3C(g)△H=+200a kJ/mol.
(4)在相同条件下,若起始时容器中加入a mol A、b mol B和c mol C,要达到t1时刻同样的平衡,a、b、c要满足的条件为a+$\frac{2}{3}$c=2.4,b+$\frac{1}{3}$c=1.2.
2.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | ag C2H4和C3H6的混合物所含原子总数为$\frac{a{N}_{A}}{14}$ | |
| B. | 0.5mol/L MgCl2溶液,含有Cl-离子数为NA | |
| C. | 10 mL质量分数为98%的H2SO4,用水稀释至100 mL,H2SO4的质量分数为9.8% | |
| D. | 300 mL 2 mol/L蔗糖溶液中所含分子数大于0.6NA |
9.下列说法正确的是( )
| A. | 溶度积就是溶解平衡时难溶电解质在溶液中的各离子浓度的乘积 | |
| B. | 溶度积常数是不受任何条件影响的常数,简称溶度积 | |
| C. | 可用离子积Qc与溶度积Ksp的比较来判断沉淀溶解平衡进行的方向 | |
| D. | 所有物质的溶度积都是随温度的升高而增大的 |
19.铝土矿的主要成分是Al2O3、Fe2O3、SiO2等,从铝土矿冶炼Al2O3的流程如图:
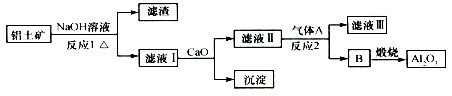
下列说法正确的是( )

下列说法正确的是( )
| A. | 气体A一定为HCl | B. | 滤液Ⅰ中溶质可能含NaAlO2 | ||
| C. | 沉淀的主要成分不是硅酸钙 | D. | 反应1、反应2均是氧化还原反应 |
6.下列反应中,最终能生成+3价铁的化合物的是( )
①铁粉和稀盐酸②过量铁和稀硝酸③过量铁和FeCl3④氯水和FeCl2⑤FeO和稀硝酸⑥铁粉和足量稀硝酸 ⑦铁片投入CuSO4溶液⑧铁在Cl2中燃烧.
①铁粉和稀盐酸②过量铁和稀硝酸③过量铁和FeCl3④氯水和FeCl2⑤FeO和稀硝酸⑥铁粉和足量稀硝酸 ⑦铁片投入CuSO4溶液⑧铁在Cl2中燃烧.
| A. | ②③④⑥ | B. | ④⑤⑥⑧ | C. | ③④⑥⑧ | D. | ②③⑤⑥ |
1.一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如图所示.已知:pM=-lg c(M),p(CO32-)=-lg c(CO32-).下列说法正确的是( )
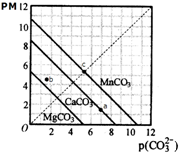

| A. | a点可表示CaCO3的饱和溶液,且c(Ca2+)<c(CO32-) | |
| B. | b点可表示MgCO3的不饱和溶液,且c(Mg2+)>c(CO32-) | |
| C. | c可表示MnCO3的饱和溶液,且c(Mn2+)=c(CO32-) | |
| D. | MgCO3、CaCO3、MnCO3的Ksp依次增大 |
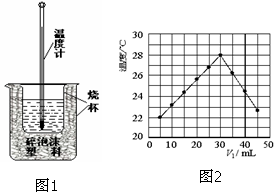 用稀盐酸与稀NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用稀盐酸与稀NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: