题目内容
在周期表中,同主族元素化学性质相似,但是也发现有些元素的化学性质和它在周期表中左上方或右下方另一主族元素性质相似,如Li与Mg,Be与Al等.这称为对角线规则,请回答:
(1)锂在空气中燃烧除生成 外,也生成微量的 .
(2)Be与NaOH溶液反应(生成Na2BeO2)的化学方程式为 .
(3)Mg(OH)2与Be(OH)2可用试剂 鉴别,其离子方程式为 .
(1)锂在空气中燃烧除生成
(2)Be与NaOH溶液反应(生成Na2BeO2)的化学方程式为
(3)Mg(OH)2与Be(OH)2可用试剂
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:(1)Mg和Li位于对角线位置,性质相似,结合Mg的性质解答;
(2)Be与Al处于对角线物质,性质相似,铍与氢氧化钠溶液反应生成Na2BeO2与氢气;
(3)Be(OH)2与氢氧化铝性质相似,为两性氢氧化物,根据两性氢氧化物能和碱(强碱)反应生成盐和水的,而氢氧化镁不反应,以此进行鉴别.
(2)Be与Al处于对角线物质,性质相似,铍与氢氧化钠溶液反应生成Na2BeO2与氢气;
(3)Be(OH)2与氢氧化铝性质相似,为两性氢氧化物,根据两性氢氧化物能和碱(强碱)反应生成盐和水的,而氢氧化镁不反应,以此进行鉴别.
解答:
解:(1)Mg能与空气中的氧气、氮气、二氧化碳反应,类比迁移,则锂在空气中燃烧的产物有Li2O和Li3N,Li2O为主要产物,故答案为:Li2O;Li3N;
(2)Be与Al处于对角线物质,性质相似,铍与氢氧化钠溶液反应生成Na2BeO2与氢气,反应方程式为:Be+2 NaOH═Na2BeO2+H2↑,故答案为:Be+2 NaOH═Na2BeO2+H2↑;
(3)Be(OH)2与氢氧化铝性质相似,为两性氢氧化物,能和NaOH溶液反应生成盐和水的,而氢氧化镁不反应,反应离子方程式为:Be(OH)2+2OH-═BeO22-+2H2O,
故答案为:NaOH溶液;Be(OH)2+2OH-═BeO22-+2H2O.
(2)Be与Al处于对角线物质,性质相似,铍与氢氧化钠溶液反应生成Na2BeO2与氢气,反应方程式为:Be+2 NaOH═Na2BeO2+H2↑,故答案为:Be+2 NaOH═Na2BeO2+H2↑;
(3)Be(OH)2与氢氧化铝性质相似,为两性氢氧化物,能和NaOH溶液反应生成盐和水的,而氢氧化镁不反应,反应离子方程式为:Be(OH)2+2OH-═BeO22-+2H2O,
故答案为:NaOH溶液;Be(OH)2+2OH-═BeO22-+2H2O.
点评:本题考查元素周期表和周期律的综合应用,难度中等,为高考常见题型,侧重于学生自学能力及类比解决问题的能力.

练习册系列答案
相关题目
下列化学用语的表达,正确的是( )
| A、氮气的电子式:N??N |
| B、乙烯的结构简式:CH2CH2 |
| C、二氧化碳分子的结构式:O-C-O |
D、CH4分子的球棍模型: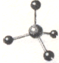 |
室温下向10mLpH=3的醋酸溶液中加水稀释后,下列说法正确的是( )
| A、溶液中导电粒子的数目减少 |
| B、再加入10mLpH=11的NaOH溶液,混合液的pH=7 |
| C、溶液中c(OH-)增大 |
| D、醋酸的电离程度增大,c(H+)亦增大 |