题目内容
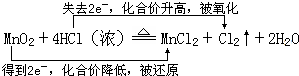
11.已知实验室制备氯气的反应为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,当生成7.1gCl2时,被氧化的HCl的质量是( )| A. | 3.65g | B. | 7.3g | C. | 10.95g | D. | 14.6g |
分析 反应中HCl中的Cl元素的化合价由-1价升高为0,被氧化生成Cl2,根据原子守恒计算.
解答 解:反应中HCl中的Cl元素的化合价由-1价升高为0,被氧化生成Cl2,2molHCl被氧化生成1mol氯气,已知生成7.1gCl2时,被氧化的HCl为$\frac{73}{71}$×7.1g=7.3g;
故选B.
点评 本题考查学生根据化学方程式的计算能力,注意氧化还原反应中,化合价升高元素被氧化,化合价降低元素被还原这一基本知识,题目难度不大,注意原子守恒在计算中的应用.

练习册系列答案
相关题目
13.化学与人类社会的生产、生活有着密切联系.下列叙述中正确的是( )
| A. | 苹果放在空气中久置变黄和纸张久置变黄原理相似 | |
| B. | 高温或日常用的消毒剂可使禽流感病毒蛋白质变性 | |
| C. | 钢铁制品和铜制品既能发生吸氧腐蚀又能发生析氢腐蚀 | |
| D. | 误食重金属盐引起人体中毒,可喝大量的食盐水解毒 |
11.已知氯仿通常是无色液体,不溶于水,密度约为水的1.5倍,沸点为61.2℃.要从水与氯仿的混合物中分离出氯仿,最合适的方法是( )
| A. | 蒸馏 | B. | 分液 | C. | 重结晶 | D. | 过滤 |
16.下列说法正确的是( )
| A. | 溶液和胶体的本质区别是丁达尔效应 | |
| B. | 液氨、氨水属于纯净物,盐酸和豆浆属于混合物 | |
| C. | 胶体区别于其它分散系的本质特征是粒子大小 | |
| D. | 能进行“交叉分类”的就不能进行“树状分类” |
1.25℃时,Kw=1.0×10-14;100℃时,Kw=1×10-12,下列说法正确的是( )
| A. | 100℃时,pH=10的NaOH溶液和pH=2的H2SO4恰好中和,所得溶液的pH=7 | |
| B. | 25℃时,0.2 mol/L Ba(OH)2溶液和0.2 mol/L HCl等体积混合,所得溶液的pH=7 | |
| C. | 25℃时,0.2 mol/L NaOH溶液与0.2 mol/L H2SO4恰好中和,所得溶液的pH<7 | |
| D. | 25℃时,pH=12的氨水和pH=2的H2SO4等体积混合,所得溶液的pH>7 |
 .
.