题目内容
1.25℃时,Kw=1.0×10-14;100℃时,Kw=1×10-12,下列说法正确的是( )| A. | 100℃时,pH=10的NaOH溶液和pH=2的H2SO4恰好中和,所得溶液的pH=7 | |
| B. | 25℃时,0.2 mol/L Ba(OH)2溶液和0.2 mol/L HCl等体积混合,所得溶液的pH=7 | |
| C. | 25℃时,0.2 mol/L NaOH溶液与0.2 mol/L H2SO4恰好中和,所得溶液的pH<7 | |
| D. | 25℃时,pH=12的氨水和pH=2的H2SO4等体积混合,所得溶液的pH>7 |
分析 A.100℃时,pH=10的NaOH溶液中c(OH-)=0.01mol/L,pH=2的H2SO4恰好中和,溶液为中性;
B.等体积等浓度混合后,碱过量;
C.恰好中和生成醋酸钠,水解显碱性;
D.25℃时,pH=12的氨水,碱的浓度大于0.01mol/L,pH=2的H2SO4中c(H+)=0.01mol/L,等体积混合,碱过量.
解答 解:A.100℃时,pH=10的NaOH溶液中c(OH-)=0.01mol/L,与pH=2的H2SO4溶液中氢离子浓度为0.01mol/L,恰好中和时溶液为中性,其pH=6,故A错误;
B.0.2mol•L-1Ba(OH)2溶液和0.2mol•L-1HCl等体积混合,碱过量,反应后溶液的pH>7,故B错误;
C.25℃时,0.2mol•L-1NaOH溶液与0.2mol•L-1CH3COOH恰好中和生成醋酸钠,水解显碱性,则所得溶液的pH>7,故C错误;
D.25℃时,pH=12的氨水,碱的浓度大于0.01mol/L,pH=2的H2SO4中c(H+)=0.01mol/L,等体积混合,碱过量,所得溶液的pH>7,故D正确;
故选D.
点评 本题考查酸碱混合溶液酸碱性的判断及pH的计算,题目难度中等,注意100℃时中性溶液的pH=6为解答的易错点,明确pH与浓度的关系是解答本题的关键,试题培养了学生灵活应用能力.

练习册系列答案
相关题目
11.已知实验室制备氯气的反应为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,当生成7.1gCl2时,被氧化的HCl的质量是( )
| A. | 3.65g | B. | 7.3g | C. | 10.95g | D. | 14.6g |
12.如图是某校实验小组设计的一套原电池装置,下列有关描述不正确的是( )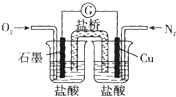

| A. | 石墨的电极反应:O2+2H20+4e-═4OH- | |
| B. | 此装置能将化学能转变为电能 | |
| C. | 电子由Cu电极经导线流向石墨电极 | |
| D. | 电池总反应:2Cu+O2+4HCl═2CuCl2+2H20 |
16.下列检验某溶液中所含离子的实验方案正确的是( )
| A. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32- | |
| B. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- | |
| C. | 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ | |
| D. | 加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+ |
6.下列做法存在安全隐患的是( )
①将水沿烧杯内壁加入浓硫酸中,并不断搅拌
②实验室制取O2时,先撤导气管再撤酒精灯
③取用金属钠或钾做完实验后,将剩余药品放回原瓶
④夜间煤气发生泄漏时,应立即开灯检查煤气泄漏的原因,然后打开所有的门窗通风
⑤油锅起火可用水灭火.
①将水沿烧杯内壁加入浓硫酸中,并不断搅拌
②实验室制取O2时,先撤导气管再撤酒精灯
③取用金属钠或钾做完实验后,将剩余药品放回原瓶
④夜间煤气发生泄漏时,应立即开灯检查煤气泄漏的原因,然后打开所有的门窗通风
⑤油锅起火可用水灭火.
| A. | ①④⑤ | B. | ①②③④ | C. | ①②③④⑤ | D. | 全部 |
13.设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 常温常压下,11.2 L氧气所含的分子数为NA | |
| B. | 1.8 g 的NH4+中含有的电子数为NA | |
| C. | 常温常压下,48 g O3含有的氧原子数为NA | |
| D. | 24 g金属镁变为镁离子时失去的电子数为NA |
11.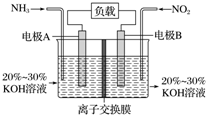 利用反应6NO2+8NH3═7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示,下列说法不正确的是( )
利用反应6NO2+8NH3═7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示,下列说法不正确的是( )
 利用反应6NO2+8NH3═7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示,下列说法不正确的是( )
利用反应6NO2+8NH3═7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示,下列说法不正确的是( )| A. | 电子从右侧电极经过负载后流向左侧电极 | |
| B. | 为使电池持续放电,离子交换膜需选用阴离子交换膜 | |
| C. | 电极A极反应式为2NH3-6e-+6OH-═N2+6H2O | |
| D. | 当有4.48 L NH3 (标准状况)反应时,转移电子为0.6 mol |