题目内容
17.下列说法或表示正确的是( )| A. | 若将等量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 | |
| B. | 由“c(石墨)=c(金刚石)△H=+1.9KJ/mol”可知,金刚石没有石墨稳定 | |
| C. | 在稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H1,CH3COOH(aq)+OH-(aq)═H2O(l)+CH3COO-(aq)△H2,则△H1>△H2 | |
| D. | 在101KPa时,2gH2完全燃烧生成液态水,放出285.8KJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)═2H2O(l)△H=285.8KJ/mol |
分析 A.固体转化为气体吸收能量;
B.物质的总能量越高,越不稳定;
C.中和反应为放热反应,醋酸电离吸收热量,注意焓变为负值;
D.2g氢气为1mol,如2mol氢气完全燃烧,应生成571.6kJ,且焓变为负值.
解答 解:A.固体转化为气体吸收能量,气体燃烧放出较多的热量,故A错误;
B.石墨转化为金刚石吸收能量,石墨能量较低,石墨较稳定,故B正确;
C.中和反应为放热反应,醋酸电离吸收热量,注意焓变为负值,醋酸放出的热量较少,反应热较大,故C错误;
D.2g氢气为1mol,如2mol氢气完全燃烧,应生成571.6kJ,且焓变为负值,热化学方程式为2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ/mol,故D错误.
故选B.
点评 本题考查反应热与焓变,为高频考点,侧重于学生的分析能力的考查,注意把握相关概念的理解,难度不大,本题注意弱电解质的电离特点以及反应热比较的角度.

练习册系列答案
相关题目
13.NaCl是一种化工原料,可以制备一系列物质,如图所示.下列说法正确的是( )
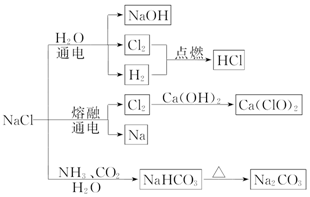

| A. | 25℃时,NaHCO3在水中的溶解度比 Na2CO3的大 | |
| B. | 石灰乳与 Cl2 的反应中,Cl2 既是氧化剂,又是还原剂 | |
| C. | 常温下干燥的 Cl2 能用钢瓶贮运,所以 Cl2 不与铁反应 | |
| D. | 图示转化反应都是氧化还原反应 |
8.AlPO4的沉淀溶解平衡曲线如图所示(T2>T1).下列说法正确的是( )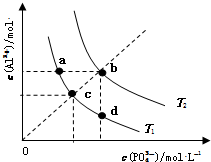

| A. | 图象中四个点的Ksp:a=b>c>d | B. | AlPO4在b点对应的溶解度大于c点 | ||
| C. | AlPO4(s)→Al3+(aq)+PO43-(aq)△H<0 | D. | 升高温度可使d点移动到b点 |
5.下列说法错误的是( )
| A. | 氯气的CCl4溶液不能使干燥红色布条褪色 | |
| B. | 通过化学变化可以实现16O与18O间的相互转化 | |
| C. | 为了便于运输和使用,可以将液氯储存在钢瓶(主要成分为铁)中 | |
| D. | 700℃时,4Na+CCl4=C+4NaCl,该反应属于置换反应 |
12.下列能用勒夏特列原理解释的是( )
| A. | 高温及加入催化剂都能使合成氨的反应速率加快 | |
| B. | H2、I2、HI平衡时的混合气体加压后颜色变深 | |
| C. | SO2催化氧化生成SO3的反应,往往需要使用催化剂 | |
| D. | 红棕色的NO2加压后颜色先变深后变浅 |
2.下列离子方程式正确的是( )
| A. | 硫酸镁溶液跟氢氧化钡溶液反应:SO42-+Ba2+=BaSO4↓ | |
| B. | 碳酸钠溶液与石灰乳的反应:CO32-+Ca2+═CaCO3↓ | |
| C. | 盐酸与氢氧化铁反应:3H++Fe(OH)3=Fe3++3H2O | |
| D. | NaOH溶液中加入醋酸:OH-+H+=H2O |
9.以下关于混合物分离提纯操作或原理说法正确的是( )
| A. | 实验室中用含有Ca2+、Mg2+、Cl-的自来水制取蒸馏水,可采用蒸馏的方法 | |
| B. | 用CCl4萃取碘水的实验中,振荡静置后,上层为紫红色溶液 | |
| C. | 利用植物油的密度比水小的原理,可用分液的方法分离这两种液体混合物 | |
| D. | 蒸馏时,温度计的水银球应充分接触溶液 |
7.在无色透明的水溶液中能大量共存的一组离子是( )
| A. | Na+、Ag+、Cl-、CO32- | B. | H+、Na+、Fe2+、MnO4- | ||
| C. | K+、Ca2+、Cl-、NO3- | D. | K+、NH4+、OH-、SO42- |