题目内容
5.下列说法错误的是( )| A. | 氯气的CCl4溶液不能使干燥红色布条褪色 | |
| B. | 通过化学变化可以实现16O与18O间的相互转化 | |
| C. | 为了便于运输和使用,可以将液氯储存在钢瓶(主要成分为铁)中 | |
| D. | 700℃时,4Na+CCl4=C+4NaCl,该反应属于置换反应 |
分析 A、氯气不能使干燥红色布条褪色;
B、16O与18O之间的转化是原子核的变化;
C、干燥的氯气和钢不反应;
D、置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应.
解答 解:A、氯气不能使干燥红色布条褪色,而四氯化碳与氯气不反应,故A正确;
B、16O与18O之间的转化,属于核变化,不是化学变化,故B错误;
C、干燥的氯气和钢不反应,可储存在钢瓶中,故C正确;
D、该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应,故D正确;
故选:B.
点评 本题考查酸碱盐和氧化物的判断、酒精和甘油鉴别、同位素之间的转化、化学键的判断等,知识点较多,难度不大.

练习册系列答案
相关题目
16.根据所学知识填空:(1)已知某反应的各物质浓度数据如下:
aA(g)+bB(g)?2C(g)
则①a=3,b=1; ②2s内B的反应速率=0.1mol•L-1•s-1.
(2)由碳棒、铁片和200mL 1.5mol•L-1的稀硫酸组成的原电池中,当在碳棒上产生气体3.36L(标准状况)时,求:①有1.806×1023个电子通过了电线(NA=6.02×1023 mol-1).
②此时溶液中H+的物质的量浓度为1.5mol•L-1 (不考虑溶液体积变化).
aA(g)+bB(g)?2C(g)
| 起始浓度(mol/L) | 1.5 | 1.0 | 0 |
| 2s末浓度(mol/L) | 0.9 | 0.8 | 0.4 |
(2)由碳棒、铁片和200mL 1.5mol•L-1的稀硫酸组成的原电池中,当在碳棒上产生气体3.36L(标准状况)时,求:①有1.806×1023个电子通过了电线(NA=6.02×1023 mol-1).
②此时溶液中H+的物质的量浓度为1.5mol•L-1 (不考虑溶液体积变化).
20.已知反应:2NO2(红棕色)?N204(无色)△H<0.将一定量的NO2充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小).下列说法正确的是( )
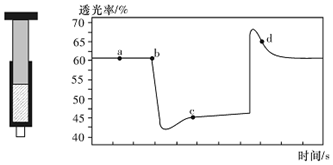

| A. | b点的操作是拉伸注射器 | |
| B. | d点:v(正)>v(逆) | |
| C. | c点与a点相比,c(N02)增大,c(N204)减小,若容器绝热则平衡常数Ka>Kc | |
| D. | 若不忽略体系温度变化,且没有能量损失,则T(b)<T(c) |
10.下列分散系不属于胶体的是( )
| A. | 纯净空气 | B. | 鸡蛋清水溶液 | C. | 牛奶 | D. | 淀粉溶液 |
17.下列说法或表示正确的是( )
| A. | 若将等量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 | |
| B. | 由“c(石墨)=c(金刚石)△H=+1.9KJ/mol”可知,金刚石没有石墨稳定 | |
| C. | 在稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H1,CH3COOH(aq)+OH-(aq)═H2O(l)+CH3COO-(aq)△H2,则△H1>△H2 | |
| D. | 在101KPa时,2gH2完全燃烧生成液态水,放出285.8KJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)═2H2O(l)△H=285.8KJ/mol |
14.向装有乙醇的烧杯中投入一小块金属钠,下列对该实验现象的描述中正确的是( )
| A. | 钠块沉在乙醇液面的下面 | B. | 钠块熔化成小球 | ||
| C. | 钠块在乙醇的液面上游动 | D. | 钠块表面有气泡产生 |
15.向一体积为2L的恒容密闭容 器里充入1mol N2和3mol H2,在一定温度下发生反应:N2(g)+3H2(g)?2NH3(g);△H<0.10秒时达到平衡,c(NH3)为0.4mol/L.下列说法正确的是( )
| A. | 向该容器中充入N2,平衡正向移动 | |
| B. | 降低温度能使混合气体的密度增大 | |
| C. | 该反应达平衡时H2的转化率为20% | |
| D. | 研发高效催化剂可大大提高N2的转化率 |
