题目内容
8.AlPO4的沉淀溶解平衡曲线如图所示(T2>T1).下列说法正确的是( )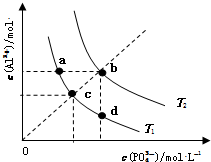
| A. | 图象中四个点的Ksp:a=b>c>d | B. | AlPO4在b点对应的溶解度大于c点 | ||
| C. | AlPO4(s)→Al3+(aq)+PO43-(aq)△H<0 | D. | 升高温度可使d点移动到b点 |
分析 A.温度相同,Ksp相同,温度越高,Ksp越大;
B.T2>T1,温度高时溶解度大;
C.沉淀溶解平衡为吸热反应;
D.升高温度,沉淀溶解平衡正向移动.
解答 解:A.温度相同,Ksp相同,温度越高,Ksp越大,则图象中四个点的Ksp:a=d=c<b,故A错误;
B.T2>T1,温度高时溶解度大,则AlPO4在b点对应的溶解度大于c点,故B正确;
C.沉淀溶解平衡为吸热反应,则AlPO4(s)→Al3+(aq)+PO43-(aq)△H>0,故C错误;
D.升高温度,沉淀溶解平衡正向移动,则升高温度Al3+、PO43-的浓度均增大,不能使d点移动到b点,故D错误;
故选B.
点评 本题考查难溶电解质的溶解平衡,为高频考点,把握图象分析、Ksp与温度有关、沉淀溶解平衡为吸热反应为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
相关题目
4.分离下列三组混合物依次采取的方法正确的是:①碳酸钙和氯化钙的溶液 ②植物油和氯化钠溶液 ③氯化钠溶液和鸡蛋清( )
| A. | 渗析、蒸馏、萃取 | B. | 分液、萃取、蒸馏 | C. | 过滤、分液、聚沉 | D. | 过滤、分液、渗析 |
5.下列物质既能通过单质间化合反应制取,也能通过单质与盐酸反应制取的是( )
| A. | CuCl2 | B. | FeCl2 | C. | FeCl3 | D. | NaCl |
16.根据所学知识填空:(1)已知某反应的各物质浓度数据如下:
aA(g)+bB(g)?2C(g)
则①a=3,b=1; ②2s内B的反应速率=0.1mol•L-1•s-1.
(2)由碳棒、铁片和200mL 1.5mol•L-1的稀硫酸组成的原电池中,当在碳棒上产生气体3.36L(标准状况)时,求:①有1.806×1023个电子通过了电线(NA=6.02×1023 mol-1).
②此时溶液中H+的物质的量浓度为1.5mol•L-1 (不考虑溶液体积变化).
aA(g)+bB(g)?2C(g)
| 起始浓度(mol/L) | 1.5 | 1.0 | 0 |
| 2s末浓度(mol/L) | 0.9 | 0.8 | 0.4 |
(2)由碳棒、铁片和200mL 1.5mol•L-1的稀硫酸组成的原电池中,当在碳棒上产生气体3.36L(标准状况)时,求:①有1.806×1023个电子通过了电线(NA=6.02×1023 mol-1).
②此时溶液中H+的物质的量浓度为1.5mol•L-1 (不考虑溶液体积变化).
20.已知反应:2NO2(红棕色)?N204(无色)△H<0.将一定量的NO2充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小).下列说法正确的是( )
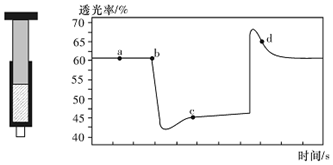

| A. | b点的操作是拉伸注射器 | |
| B. | d点:v(正)>v(逆) | |
| C. | c点与a点相比,c(N02)增大,c(N204)减小,若容器绝热则平衡常数Ka>Kc | |
| D. | 若不忽略体系温度变化,且没有能量损失,则T(b)<T(c) |
17.下列说法或表示正确的是( )
| A. | 若将等量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 | |
| B. | 由“c(石墨)=c(金刚石)△H=+1.9KJ/mol”可知,金刚石没有石墨稳定 | |
| C. | 在稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H1,CH3COOH(aq)+OH-(aq)═H2O(l)+CH3COO-(aq)△H2,则△H1>△H2 | |
| D. | 在101KPa时,2gH2完全燃烧生成液态水,放出285.8KJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)═2H2O(l)△H=285.8KJ/mol |

 .
.