题目内容
实验室需要0.1mol/L的硫酸920mL,某同学欲用密度为1.84g/cm3、溶质的质量分数为98%的浓硫酸进行配制.试回答:
(1)需选用 容量瓶(填序号).
A.50mL B.100mL C.250mL D.1000mL
(2)需量取98%浓硫酸的体积为 mL.
(3)下列关于容量瓶的使用方法中,正确的是 (填序号).
A.使用前要检验是否漏水
B.在容量瓶中直接溶解固体或稀释液体
C.溶液未经冷却即注入容量瓶中
D.向容量瓶中转移溶液时,用玻璃棒引流
(4)导致浓度偏低的原因可能是 (填序号).
A.容量瓶中原有少量的蒸馏水
B.移液时,不慎将液体流到瓶外
C.容量瓶盛过硫酸溶液,使用前未洗涤
D.定容时俯视刻度线和液面
E.未洗涤烧杯、玻璃棒.
(1)需选用
A.50mL B.100mL C.250mL D.1000mL
(2)需量取98%浓硫酸的体积为
(3)下列关于容量瓶的使用方法中,正确的是
A.使用前要检验是否漏水
B.在容量瓶中直接溶解固体或稀释液体
C.溶液未经冷却即注入容量瓶中
D.向容量瓶中转移溶液时,用玻璃棒引流
(4)导致浓度偏低的原因可能是
A.容量瓶中原有少量的蒸馏水
B.移液时,不慎将液体流到瓶外
C.容量瓶盛过硫酸溶液,使用前未洗涤
D.定容时俯视刻度线和液面
E.未洗涤烧杯、玻璃棒.
考点:配制一定物质的量浓度的溶液
专题:物质的量浓度和溶解度专题
分析:(1)选取的容量瓶规格应该等于或稍大于需要配制溶液的体积;
(2)先根据C=
计算浓硫酸的浓度,再根据浓硫酸稀释前后溶质的物质的量不变计算;
(3)根据正确使用容量瓶的操作方法判断;
(4)根据C=
判断,如果n偏小或V偏大,则配制溶液浓度偏低.
(2)先根据C=
| 103ρw |
| M |
(3)根据正确使用容量瓶的操作方法判断;
(4)根据C=
| n |
| V |
解答:
解:(1)选取的容量瓶规格应该等于或稍大于需要配制溶液的体积,实验室没有920mL容量瓶,有1000mL容量瓶,所以应该选取1000mL容量瓶,故选D;
(2)浓硫酸的浓度=C=
=
mol/L=18.4mol/L,浓硫酸稀释前后溶质的物质的量不变,设浓硫酸的体积为V,所以18.4mol/L×V=0.10mol/L×1L,V=0.0054L=5.4mL,故答案为:5.4;
(3)A.使用前要检验是否漏水,故正确;
B.容量瓶不能用来稀释浓溶液或溶解固体,只能用来配制溶液,故错误;
C.溶液未经冷却即注入容量瓶中,导致溶液体积偏小,配制浓度偏大,故错误;
D.向容量瓶中转移溶液要用玻璃棒引流,防止液体溅出,故正确;
故选AD.
(4)A.容量瓶中原有少量的蒸馏水,溶质的物质的量和溶液的体积都不变,所以配制溶液浓度无影响,故错误;
B.移液时,不慎将液体流到瓶外,溶质的物质的量偏小,配制溶液浓度偏低,故正确;
C.容量瓶盛过硫酸溶液,使用前未洗涤,溶质的物质的量偏大,配制溶液浓度偏高,故错误;
D.定容时俯视刻度线和液面,导致溶液体积偏小,配制浓度偏高,故错误;
E.未洗涤烧杯、玻璃棒,溶质的物质的量偏小,配制溶液浓度偏低,故正确;
故选BE.
(2)浓硫酸的浓度=C=
| 103ρw |
| M |
| 103×1.84×98% |
| 98 |
(3)A.使用前要检验是否漏水,故正确;
B.容量瓶不能用来稀释浓溶液或溶解固体,只能用来配制溶液,故错误;
C.溶液未经冷却即注入容量瓶中,导致溶液体积偏小,配制浓度偏大,故错误;
D.向容量瓶中转移溶液要用玻璃棒引流,防止液体溅出,故正确;
故选AD.
(4)A.容量瓶中原有少量的蒸馏水,溶质的物质的量和溶液的体积都不变,所以配制溶液浓度无影响,故错误;
B.移液时,不慎将液体流到瓶外,溶质的物质的量偏小,配制溶液浓度偏低,故正确;
C.容量瓶盛过硫酸溶液,使用前未洗涤,溶质的物质的量偏大,配制溶液浓度偏高,故错误;
D.定容时俯视刻度线和液面,导致溶液体积偏小,配制浓度偏高,故错误;
E.未洗涤烧杯、玻璃棒,溶质的物质的量偏小,配制溶液浓度偏低,故正确;
故选BE.
点评:本题考查一定物质的量浓度溶液的配制,注意容量瓶和量筒规格的选取方法及误差分析,为易错点,难度不大.

练习册系列答案
相关题目
下列结构示意图所代表的微粒中,最难发生化学反应的是( )
A、 |
B、 |
C、 |
D、 |
如图是常见四种有机物的比例模型示意图.下列说法正确的是( )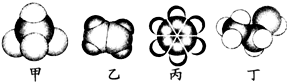

| A、甲能使酸性高锰酸钾溶液褪色 |
| B、乙可与溴水发生取代反应使溴水褪色 |
| C、丙中的碳碳键是介于碳碳单键和碳碳双键之间的独特的共价键 |
| D、丁与乙酸都能发生发生中和反应 |

 如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球的影响).则滴管和烧瓶中所用试剂不可能是( )
如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球的影响).则滴管和烧瓶中所用试剂不可能是( )