题目内容
 如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球的影响).则滴管和烧瓶中所用试剂不可能是( )
如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球的影响).则滴管和烧瓶中所用试剂不可能是( )| 甲 | 乙 | |
| A | 水和过氧化钠 | 盐酸和NH3 |
| B | 双氧水和MnO2 | 水和NO |
| C | 盐酸和NaHCO3固体 | NaOH溶液和Cl2 |
| D | 饱和食盐水和电石 | 酸性高锰酸钾溶液和SO2 |
| A、A | B、B | C、C | D、D |
考点:实验装置综合
专题:实验设计题,元素及其化合物
分析:甲装置气球膨大原因是烧瓶内有气体生成或者温度升高,使烧瓶内的压强大于外界压强;乙装置气球膨大原因是烧瓶内的气体反应或者温度降低,使烧瓶内的压强小于外界压强,结合对应物质的性质解答该题.
解答:
解:A.水和过氧化钠反应生成氧气,甲压强增大,气球胀大,乙盐酸和NH3反应生成氯化铵,压强减小,气球明显胀大,故A正确;
B.水和NO不反应,气球不变化,故B错误;
C.盐酸和NaHCO3固体生成二氧化碳气体,甲压强增大,气球胀大,NaOH溶液和Cl2反应生成氯化钠、次氯酸钠,乙压强减小,气球明显胀大,故C正确;
D.饱和食盐水和电石反应生成乙炔,饱和食盐水和电石,酸性高锰酸钾溶液和SO2反应,二氧化硫被吸收,乙压强减小,气球明显胀大,故D正确.
故选B.
B.水和NO不反应,气球不变化,故B错误;
C.盐酸和NaHCO3固体生成二氧化碳气体,甲压强增大,气球胀大,NaOH溶液和Cl2反应生成氯化钠、次氯酸钠,乙压强减小,气球明显胀大,故C正确;
D.饱和食盐水和电石反应生成乙炔,饱和食盐水和电石,酸性高锰酸钾溶液和SO2反应,二氧化硫被吸收,乙压强减小,气球明显胀大,故D正确.
故选B.
点评:本题考查了常见气体的制备原理及装置选择,为高频考点,侧重于学生的分析能力和实验能力的考查,同时考查酸、碱、盐的性质,要理解和掌握酸、碱、盐常见的化学反应,难度不大.

练习册系列答案
相关题目
自保定市被世界自然基金会选定为“中国低碳城市发展项目”的首批试点城市之后,“低碳”已经走进百姓生活、城市建设以及经济发展等各个领域,下列有关说法不正确的是( )
| A、太阳能、地热能、核能等均属于新能源 |
| B、“低碳”是指采用含碳量低的烃类化合物作燃料 |
C、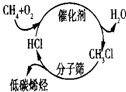 甲烷经一氯甲烷转化成低碳烯烃的途径体现了“节能减排”思想 |
| D、减少化石能源的使用能减少CO2的排放量 |
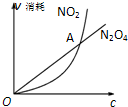 已知可逆反应:2NO2(g)N2O4(g)中,NO2、N2O4的消耗速率与其浓度存在如下关系:v(NO2)=k1?c2(NO2),v(N2O4)=k2?c(N2O4)(其中k1、k2是只与温度有关的常数),一定温度下根据上述关系式建立如图关系.下列说法正确的是( )
已知可逆反应:2NO2(g)N2O4(g)中,NO2、N2O4的消耗速率与其浓度存在如下关系:v(NO2)=k1?c2(NO2),v(N2O4)=k2?c(N2O4)(其中k1、k2是只与温度有关的常数),一定温度下根据上述关系式建立如图关系.下列说法正确的是( )| A、图中A点对应的状态表示该反应达到化学平衡 |
| B、若某温度时k1=k2,则该温度下反应的平衡常数K=0.5 |
| C、在1L密闭容器中充入1 mol NO2,平衡时:c(NO2)+c(N2O4)=1 mol?L-1 |
| D、在1L密闭容器中充入1 mol NO2,当c(NO2)=c(N2O4)时,NO2的转化率是33.3% |
下列分子中,所有原子都满足最外层为8电子结构的是( )
| A、BF3 |
| B、CF2Cl2 |
| C、HCl |
| D、PCl5 |
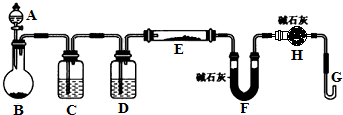 某课外小组利用H2还原黄色的WO3粉末测定W的相对原子质量,如图是测定装置的示意图.A中的试剂是盐酸.请回答下列问题:
某课外小组利用H2还原黄色的WO3粉末测定W的相对原子质量,如图是测定装置的示意图.A中的试剂是盐酸.请回答下列问题: