题目内容
6.已知X、Y、Z、W、L为五种短周期元素,非金属元素X最外层电子数与其周期序数相同,Y的最外层电子数是其所在周期数的2倍.Y在Z中充分燃烧能生成其最高价化合物YZ2.W+与Z2-具有相同的电子数.X在L中燃烧,产物XL溶于水得到一种强酸.请回答下列问题:(1)X在周期表中的位置是第一周期IA族.请写出实验室制备L单质时的尾气处理的离子方程式:Cl2+2OH-=Cl-+ClO-+H2O,
W的单质与X2Z反应的化学方程式2Na+2H2O=2NaOH+H2↑,
(2)由X分别与Y、Z形成的最简单化合物的稳定性关系为:H2O>CH4.
(3)由X、Y、Z、W组成的一种盐,在面食中有大量使用,其俗名为:小苏打,在其水溶液中滴入由X、Y、Z形成的日常生活中常见的一种酸,反应的离子方程式为:CH3COOH+HCO3-=CH3COO-+CO2↑+H2O.
分析 X、Y、Z、W、L为五种短周期元素,非金属元素X最外层电子数与其周期数相同,则X为H元素;W+与Z2-具有相同的电子数,则W处于IA族,Z处于ⅥA族,则W为Na、Z为O元素;Y在Z中充分燃烧能生成其最高价化合物YZ2,Y的最高正化合价为+4,Y的最外层电子数是其所在周期数的2倍,则BY处于第二周期,故Y为碳元素;X在L中燃烧,产物XL溶于水得到一种强酸,则L为Cl,据此解答.
解答 解:X、Y、Z、W、L为五种短周期元素,非金属元素X最外层电子数与其周期数相同,则X为H元素;W+与Z2-具有相同的电子数,则W处于IA族,Z处于ⅥA族,则W为Na、Z为O元素;Y在Z中充分燃烧能生成其最高价化合物YZ2,Y的最高正化合价为+4,Y的最外层电子数是其所在周期数的2倍,则BY处于第二周期,故Y为碳元素;X在L中燃烧,产物XL溶于水得到一种强酸,则L为Cl.
(1)X为H元素,在周期表中的位置是:第一周期IA族,实验室制备氯气单质时用氢氧化钠反应进行为期处理,反应离子方程式:Cl2+2OH-=Cl-+ClO-+H2O,W的单质与X2Z反应的化学方程式:2Na+2H2O=2NaOH+H2↑,
故答案为:第一周期IA族;Cl2+2OH-=Cl-+ClO-+H2O;2Na+2H2O=2NaOH+H2↑;
(2)由于非金属性O>C,非金属性越强,氢化物越稳定,由氢分别与碳、氧形成的最简单化合物的稳定性关系为:H2O>CH4,
故答案为:H2O>CH4;
(3)由X、Y、Z、W组成的一种盐为碳酸氢钠,在面食中有大量使用,其俗名为:小苏打,在其水溶液中滴入由X、Y、Z形成的日常生活中常见的一种酸(CH3COOH),反应的离子方程式为:CH3COOH+HCO3-=CH3COO-+CO2↑+H2O,
故答案为:小苏打;CH3COOH+HCO3-=CH3COO-+CO2↑+H2O.
点评 本题考查结构性质位置关系综合应用,关键是推断元素,注意对元素化合物性质的掌握,题目难度中等.

| A. | CS2为V形的极性分子 | |
| B. | Cl03- 的空间构型为平面三角形 | |
| C. | SF6中有6对完全相同的成键电子对 | |
| D. | SiF4和SO32- 的中心原子均为sp3杂化 |
| A. | 6:6:1 | B. | 6:3:1 | C. | 3:3:1 | D. | 9:3:1 |
| n(SO2)/mol | n(O2)/mol | n(SO3)/mol | |
| A | 2.0 | 1.0 | 0 |
| B | 1.0 | 0 | 1.0 |
| C | 0.20 | 0.10 | 1.80 |
| D | 0 | 0 | 2.0 |
| A. | A | B. | B | C. | C | D. | D |
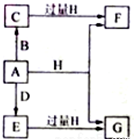 A、B、D是由常见的短周期非金属元素形成的单质,常温下A是淡黄色粉末,B、D是气体,F、G、H的焰色反应均为黄色,水溶液均显碱性,E有漂白性.它们之间的转化关系如图所示(部分产物及反应条件已略去),回答下列问题.
A、B、D是由常见的短周期非金属元素形成的单质,常温下A是淡黄色粉末,B、D是气体,F、G、H的焰色反应均为黄色,水溶液均显碱性,E有漂白性.它们之间的转化关系如图所示(部分产物及反应条件已略去),回答下列问题. .
.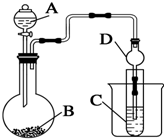 某兴趣小组设计如下实验来证明同周期元素Cl和S的非金属性强弱.
某兴趣小组设计如下实验来证明同周期元素Cl和S的非金属性强弱. ;
; ;
; ;
; ;
;