题目内容
电化学降解NO3-的原理如图所示.下列说法中不正确的是( )


| A、铅蓄电池的A极为正极,电极材料为PbO2 |
| B、铅蓄电池工作过程中负极质量增加 |
| C、该电解池的阴极反应为:2NO3-+6H2O+10e-=N2↑+12OH- |
| D、若电解过程中转移2moL电子,则交换膜两侧电解液的质量变化差(△m左-△m右)为10.4g |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A.该装置中,硝酸根离子得电子发生还原反应,则Ag-Pt电极为阴极、Pt电极为阳极,连接阳极的电极为正极;
B.铅蓄电池工作过程中负极为Pb失电子生成硫酸铅;
C.阴极上硝酸根离子得电子发生还原反应;
D.转移2mol电子时,阳极(阳极反应为H2O失电子氧化为O2和H+)消耗1mol水,产生2molH+进入阴极室,阳极室质量减少18g;阴极室中放出0.2molN2(5.6g),同时有2molH+(2g)进入阴极室;
B.铅蓄电池工作过程中负极为Pb失电子生成硫酸铅;
C.阴极上硝酸根离子得电子发生还原反应;
D.转移2mol电子时,阳极(阳极反应为H2O失电子氧化为O2和H+)消耗1mol水,产生2molH+进入阴极室,阳极室质量减少18g;阴极室中放出0.2molN2(5.6g),同时有2molH+(2g)进入阴极室;
解答:
解:A.根据图知,电解槽右边部分N元素化合价由+5价变为0价,所以硝酸根离子发生还原反应,则Ag-Pt电极为阴极、Pt电极为阳极,所以A是正极、电极材料为PbO2,故A正确;
B.铅蓄电池工作过程中负极为Pb失电子生成硫酸铅,所以负极质量增加,故B正确;
C.阴极上硝酸根离子得电子发生还原反应,电极反应式为2NO3-+6H2O+10e-=N2↑+12OH-,故C正确;
D.转移2mol电子时,阳极(阳极反应为H2O失电子氧化为O2和H+)消耗1mol水,产生2molH+进入阴极室,阳极室质量减少18g;阴极的电极反应式为2NO3-+6H++10e-=N2↑+6OH-,转移2mol电子,阴极室中放出0.2molN2(5.6g),同时有2molH+(2g)进入阴极室,因此阴极室质量减少3.6g,故膜两侧电解液的质量变化差(△m左-△m右)=18g-3.6g=14.4g,故D错误;
故选D.
B.铅蓄电池工作过程中负极为Pb失电子生成硫酸铅,所以负极质量增加,故B正确;
C.阴极上硝酸根离子得电子发生还原反应,电极反应式为2NO3-+6H2O+10e-=N2↑+12OH-,故C正确;
D.转移2mol电子时,阳极(阳极反应为H2O失电子氧化为O2和H+)消耗1mol水,产生2molH+进入阴极室,阳极室质量减少18g;阴极的电极反应式为2NO3-+6H++10e-=N2↑+6OH-,转移2mol电子,阴极室中放出0.2molN2(5.6g),同时有2molH+(2g)进入阴极室,因此阴极室质量减少3.6g,故膜两侧电解液的质量变化差(△m左-△m右)=18g-3.6g=14.4g,故D错误;
故选D.
点评:本题考查了电解原理,根据N元素化合价变化确定阴阳极、正负极,难点是电极反应式的书写,易错选项是D,注意氢离子还进入阴极室,很多同学往往只考虑析出的气体而导致错误,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
分类法在化学的发展中起到了重要作用,下列有关分类标准的叙述合理的是( )
| A、根据化学反应中的热效应将化学反应分为放热反应和吸热反应 |
| B、根据水溶液能否导电将化合物分为电解质和非电解质 |
| C、根据氧化物的组成将氧化物分为酸性氧化物、碱性氧化物和两性氧化物 |
| D、根据分散质和分散剂的聚集状态将分散系为浊液、胶体和溶液 |
A、B、C、D四种气体之间可发生反应:aA+bB?cC+d D,该反应在一定条件下建立平衡,改变条件,经足够长的时间后,体系发生了下列各种变化,其中能表明该平衡一定发生了转移的是( )
| A、混合气的密度增大了 |
| B、混合体系的压强增大了 |
| C、正逆反应的速率相等,且都比原平衡状态的速率增大了 |
| D、A气体在混合气中的含量升高了 |
对于Zn(s)+H2SO4(aq)═ZnSO4(aq)+H2(g)△H=?的化学反应,下列叙述不正确的是( )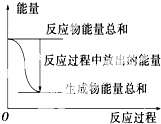

| A、反应过程中能量关系如上图表示,则该反应为放热反应 |
| B、若将其设计为原电池,当有32.5 g锌溶解时,正极放出气体一定为11.2 L |
| C、化学反应的焓变与反应方程式的计量数有关 |
| D、若将该反应设计成原电池,锌为负极 |
下列说法正确的是( )
| A、最外层电子数是核外电子总数的1/5的原子和价电子排布式为4s24p5的两个微粒属于同种元素的原子 |
| B、在一个基态的多电子的原子中,不能有两个能量完全相同的电子 |
| C、原子核外的M层上的S能级和P能级都填满电子,而d轨道上尚未有电子的两种原子一定属于同一周期 |
| D、PCl3、BeCl2、BF3中所有原子均满足最外层8电子结构 |
有2份质量分数不同的NaHCO3和NaOH的混合物,将它们分别用酒精灯加热至恒重测得的数据如下:经分析得到的15.600g固体是纯净物.则下列叙述正确的是( )
| 第1份 | 第2份 | |
| 混合物质量(g) | 9.2 | 18.4 |
| 反应后固体质量(g) | 8.3 | 15.6 |
| A、本次实验至少要进行6次称重 |
| B、第1份混合物中NaOH的质量分数更大 |
| C、根据表中数据不能计算出第1份混合物中NaHCO3的质量分数 |
| D、第2份混合物中NaOH的质量分数小于0.32 |