题目内容
3.01×1023个H2O的物质的量为 ;质量为 .
考点:物质的量的相关计算
专题:计算题
分析:依据n=
=
计算得到.
| N |
| NA |
| m |
| M |
解答:
解:3.01×1023个H2O的物质的量=
=0.5mol,质量=nM=0.5mol×18g/mol=9g;故答案为:0.5mol;9g.
| 3.01×1023 |
| 6.02×1023 |
点评:本题考查物质的量与质量、微粒数的换算关系,题目较简单.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案
相关题目
有关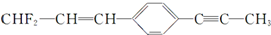 分子结构的下列叙述中,正确的是( )
分子结构的下列叙述中,正确的是( )
 分子结构的下列叙述中,正确的是( )
分子结构的下列叙述中,正确的是( )| A、除苯环外的其余碳原子有可能都在一条直线上 |
| B、所有的原子都在同一平面上 |
| C、12个碳原子不可能都在同一平面上 |
| D、12个碳原子有可能都在同一平面上 |
电化学降解NO3-的原理如图所示.下列说法中不正确的是( )


| A、铅蓄电池的A极为正极,电极材料为PbO2 |
| B、铅蓄电池工作过程中负极质量增加 |
| C、该电解池的阴极反应为:2NO3-+6H2O+10e-=N2↑+12OH- |
| D、若电解过程中转移2moL电子,则交换膜两侧电解液的质量变化差(△m左-△m右)为10.4g |
乙炔、苯和乙醛的混合物中w(C)=72%(w为质量分数),则w(O)是( )
| A、22% | B、19.6% |
| C、8.8% | D、4.4% |
下列说法正确的是( )
| A、将10 g CaCO3粉末加入100 mL水中,所得溶液的浓度为l mol?L-1 |
| B、将100 mL 2 mol?L-1盐酸加热蒸发至50 mL,所得溶液的浓度为4 mol?L-1 |
| C、将l0 mL l.0mol?L-1NaCl溶液与90mL水混合,所得溶液的浓度为0.1 mol?L-1 |
| D、将10 g CaO加入100 mL饱和石灰水中,充分搅拌、静置并恢复到原来的温度,所得溶液的浓度不变 |
设NA表示阿伏加德罗常数,下列说法正确的是( )
| A、18 g水中所含的电子数为10NA |
| B、1 mol氧中有2NA个氧原子 |
| C、0.3 mol?L-1Na2SO4溶液中含0.6NA个Na+ |
| D、11.2L氮气中含NA个氮原子 |
下列溶液中Cl-浓度最小的是( )
| A、100mL 0.5mol/L KClO3溶液 |
| B、200mL 2.5mol/L MgCl2溶液 |
| C、300mL 2mol/L AlCl3溶液 |
| D、400mL1mol/L 盐酸 |
Na2CO3俗名纯碱,下面是对纯碱采用不同分类法的分类,不正确的是( )
| A、Na2CO3是碳酸盐 |
| B、Na2CO3是正盐 |
| C、Na2CO3是钠盐 |
| D、Na2CO3是碱 |
取三份由NaCl、MgCl2、BaCl2溶液组成的营养液各10ml,分别加入1mol?L-1的NaOH、Na2SO4、AgNO3溶液至恰好反应,消耗溶液的体积如图所示,该营养液中钠离子的浓度为( )
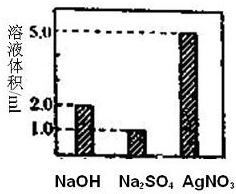

| A、0.5 mol?L-1 |
| B、0.1 mol?L-1 |
| C、1 mol?L-1 |
| D、1.5 mol?L-1 |