题目内容
A、B、C、D四种气体之间可发生反应:aA+bB?cC+d D,该反应在一定条件下建立平衡,改变条件,经足够长的时间后,体系发生了下列各种变化,其中能表明该平衡一定发生了转移的是( )
| A、混合气的密度增大了 |
| B、混合体系的压强增大了 |
| C、正逆反应的速率相等,且都比原平衡状态的速率增大了 |
| D、A气体在混合气中的含量升高了 |
考点:化学平衡移动原理
专题:
分析:A、如果两边气体计量数相等,体积可变,增大压强;
B、如果两边气体计量数相等;
C、使用正催化剂去分析;
D、A气体在混合气中的含量升高了,说明平衡向生成A的方向移动.
B、如果两边气体计量数相等;
C、使用正催化剂去分析;
D、A气体在混合气中的含量升高了,说明平衡向生成A的方向移动.
解答:
解:A、如果两边气体计量数相等,体积可变,增大压强,故A错误;
B、如果两边气体计量数相等,缩不体积,混合体系的压强增大,但平衡不移动,故B错误;
C、使用正催化剂,正逆反应的速率相等,且都比原平衡状态的速率增大了,故C错误;
D、A气体在混合气中的含量升高了,说明平衡向生成A的方向移动,故D正确;
故选D.
B、如果两边气体计量数相等,缩不体积,混合体系的压强增大,但平衡不移动,故B错误;
C、使用正催化剂,正逆反应的速率相等,且都比原平衡状态的速率增大了,故C错误;
D、A气体在混合气中的含量升高了,说明平衡向生成A的方向移动,故D正确;
故选D.
点评:本题考查了外界条件对化学平衡的影响适用范围:1、浓度对化学平衡的影响适用于气体或液体;2、压强对化学平衡的影响适用于有气体参加且反应前后气体体积变化的反应;3、温度对所有可逆反应都有影响,无论该反应放热还是吸热,题目难度中等

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列实验中,不能达到相应实验目的是( )
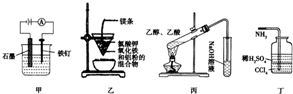

| A、装置甲:防止铁钉生锈 |
| B、装置乙:可制得金属铁 |
| C、装置丙:实验室制取乙酸乙酯 |
| D、装置丁:吸收多余的氨气 |
除去FeCl2溶液中混有的FeCl3,应选用的试剂是( )
| A、硫氰化钾溶液 | B、氢氧化钠溶液 |
| C、铜粉 | D、铁粉 |
今有HA、H2B两种弱酸,有如下关系:H2B+A-=HB-+HA B2-+HA=HB-+A-则下列说法正确的是( )
| A、H2B的电离方程式为:H2B?2H++B2- |
| B、结合质子能力由强到弱的顺序为:B2->A->HB- |
| C、等物质的量浓度NaA、NaHB、Na2B三种盐的水溶液,NaA碱性最强 |
| D、等pH的HA、H2B两种溶液中,水的电离出的氢离子前者大于后者 |
下列关于电解质的电离平衡状态的叙述中,正确的是( )
| A、弱电解质的电离达到平衡状态后,电离就停止了 |
| B、分子的消耗速率和离子的生成速率相等,说明弱电解质的电离达到平衡状态 |
| C、弱电解质的电离达到平衡状态后,分子和离子的浓度相等 |
| D、弱电解质的电离达到平衡状态后,外界条件改变,电离平衡可能要发生移动 |
电化学降解NO3-的原理如图所示.下列说法中不正确的是( )


| A、铅蓄电池的A极为正极,电极材料为PbO2 |
| B、铅蓄电池工作过程中负极质量增加 |
| C、该电解池的阴极反应为:2NO3-+6H2O+10e-=N2↑+12OH- |
| D、若电解过程中转移2moL电子,则交换膜两侧电解液的质量变化差(△m左-△m右)为10.4g |
下列叙述正确的是( )
| A、反应NH3(g)+HCl(g)?NH4C1(s)△H<O在任何条件下均能自发进行 |
| B、对于可逆反应N2(g)+3H2(g)?2NH3(g),增大氮气浓度可增加活化分子百分数,从而使反应速率增加 |
| C、将A1C13溶液和NaAlO2溶液分别蒸干后灼烧,所得固体产物均为A1203 |
| D、恒容密闭容器中进行的反应3A(g)?B(g)+c(g),在其他条件不变的情况下,再充入一定量的A气体,A的转化率将增大 |
下列说法正确的是( )
| A、将10 g CaCO3粉末加入100 mL水中,所得溶液的浓度为l mol?L-1 |
| B、将100 mL 2 mol?L-1盐酸加热蒸发至50 mL,所得溶液的浓度为4 mol?L-1 |
| C、将l0 mL l.0mol?L-1NaCl溶液与90mL水混合,所得溶液的浓度为0.1 mol?L-1 |
| D、将10 g CaO加入100 mL饱和石灰水中,充分搅拌、静置并恢复到原来的温度,所得溶液的浓度不变 |