题目内容
18.鉴别乙醇和汽油,最简单的方法是( )| A. | 加金属钠,有气体产生的是乙醇 | |
| B. | 加水,互溶的是乙醇 | |
| C. | 点燃,容易燃烧的是乙醇 | |
| D. | 和浓硫酸混合共热至170℃,有乙烯产生的是乙醇 |
分析 乙醇含-OH,汽油的成分为烃,汽油不溶于水,而乙醇与水互溶,以此来解答.
解答 解:A.乙醇与Na反应生成气体,而汽油不能,但方法不最简单,故A不选;
B.加水,互溶的为乙醇,分层的为汽油,可鉴别,故B选;
C.点燃,均燃烧,不易鉴别,故C不选;
D.乙醇消去反应实验较复杂,汽油不能,可鉴别,但方法较复杂,故D不选;
故选B.
点评 本题考查物质的鉴别和检验,为高频考点,把握有机物的性质、性质差异及发生的反应为解答的关键,注意信息中最简单方法的限定,题目难度不大.

练习册系列答案
 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案
相关题目
9.短周期元素a、b、c、d的原子序数依次增大.c、a、b最外层电子数为等差数列.公差为2.a、c的价电子数之和为6.d的核外电子数等于b的核外电子数加8.下列叙述错误的是( )
| A. | a和b可形成气态化合物 | |
| B. | c的原子半径小于d的原子半径 | |
| C. | b和c形成的化合物为离子化合物 | |
| D. | a和d最高价氧化物的水化物均呈酸性 |
6.常温下,下列溶液中c(H+)最小的是( )
| A. | 0.01mol•L-1的H2SO4溶液 | B. | 0.01mol•L-1的Ba(OH)2溶液 | ||
| C. | c(OH-)=1×10-11mol•L-1的溶液 | D. | c(H+)=1×10-12mol•L-1的溶液 |
3.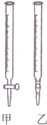 某学生用0.1000mol•L-1标准NaOH溶液滴定未知浓度的盐酸,其操作可分解为如下几步:
某学生用0.1000mol•L-1标准NaOH溶液滴定未知浓度的盐酸,其操作可分解为如下几步:
A.移取25.0mL待测盐酸溶液注入洁净的锥形瓶中,并加入2~3滴酚酞溶液
B.用标准NaOH溶液润洗滴定管2~3次
C.把盛有标注NaOH溶液的滴定管固定好,挤压玻璃球,使滴定管尖嘴充满溶液
D.取标准NaOH溶液注入碱式滴定管到“0”刻度以上2~3cm
E.调节液面值“0”或“0”刻度以下,记下读数
F.把锥形瓶放在滴定管的下面,进行滴定操作到终点,并记下滴定管液面的读数
回答下列问题:
(1)如图中属于酸式滴定管的甲(选填“甲”、“乙”).
(2)正确操作步骤的顺序是BDCEAF(填字母序号).
(3)上述B步操作的目的是防止滴定管内壁附着的水将标准溶液稀释而带来误差.
(4)判断到达滴定终点的实验现象是溶液由无色变为浅红色,且半分钟内不褪色.
(5)下列哪些操作会使测定结果偏高AC(填序号).
A.碱式滴定管用蒸馏水洗净后未用标准液润洗
B.在振荡锥形瓶时不慎将瓶内溶液溅出
C.滴定前碱式滴定管尖端气泡未排除,滴定后气泡消失
D.滴定前读数正确,滴定后俯视滴定管读数
(6)若平行实验三次,记录的数据如下表
试计算待测盐酸的物质的量浓度为0.0800mol•L-1.
 某学生用0.1000mol•L-1标准NaOH溶液滴定未知浓度的盐酸,其操作可分解为如下几步:
某学生用0.1000mol•L-1标准NaOH溶液滴定未知浓度的盐酸,其操作可分解为如下几步:A.移取25.0mL待测盐酸溶液注入洁净的锥形瓶中,并加入2~3滴酚酞溶液
B.用标准NaOH溶液润洗滴定管2~3次
C.把盛有标注NaOH溶液的滴定管固定好,挤压玻璃球,使滴定管尖嘴充满溶液
D.取标准NaOH溶液注入碱式滴定管到“0”刻度以上2~3cm
E.调节液面值“0”或“0”刻度以下,记下读数
F.把锥形瓶放在滴定管的下面,进行滴定操作到终点,并记下滴定管液面的读数
回答下列问题:
(1)如图中属于酸式滴定管的甲(选填“甲”、“乙”).
(2)正确操作步骤的顺序是BDCEAF(填字母序号).
(3)上述B步操作的目的是防止滴定管内壁附着的水将标准溶液稀释而带来误差.
(4)判断到达滴定终点的实验现象是溶液由无色变为浅红色,且半分钟内不褪色.
(5)下列哪些操作会使测定结果偏高AC(填序号).
A.碱式滴定管用蒸馏水洗净后未用标准液润洗
B.在振荡锥形瓶时不慎将瓶内溶液溅出
C.滴定前碱式滴定管尖端气泡未排除,滴定后气泡消失
D.滴定前读数正确,滴定后俯视滴定管读数
(6)若平行实验三次,记录的数据如下表
| 滴定次数 | 待测溶液的体积(/mL) | 标准NaOH溶液的体积 | |
| 滴定前读数(/mL) | 滴定后读数(/mL) | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 0.00 | 22.99 |
| 3 | 25.00 | 0.20 | 20.19 |
10.室温下,下列叙述正确的是( )
| A. | pH=2的HA酸溶液与pH=12的MOH碱溶液以任意比混合:c(OH-)+c(M+)=c(H+)+c(A-) | |
| B. | 将物质的量浓度均为0.1mol•L-1的Na2CO3溶液和NaHCO3溶液等体积混合所得溶液中:2c(OH-)-2c(H+)=3c(H2CO3)+c(HCO${\;}_{3}^{-}$)-c(CO${\;}_{3}^{2-}$) | |
| C. | 等浓度、等体枳的Na2CO3和NaHCO3混合:$\frac{c(HC{O}_{3}^{-})}{c({H}_{2}C{O}_{3})}$<$\frac{c(C{O}_{3}^{2-})}{c(HC{O}_{3}^{-})}$ | |
| D. | 将足量AgCl分别放入:①5mL水,②10mL0.2mol/LMgCl2,③20mL0.3mol/L盐酸中溶解至饱和,c(Ag+):①>②>③ |
7. 用0.1mol•L-1NaOH溶液滴定10mL0.1mol•L-1H2A溶液,溶液的pH与NaOH溶液的体积关系如图所示.下列说法错误的是( )
用0.1mol•L-1NaOH溶液滴定10mL0.1mol•L-1H2A溶液,溶液的pH与NaOH溶液的体积关系如图所示.下列说法错误的是( )
 用0.1mol•L-1NaOH溶液滴定10mL0.1mol•L-1H2A溶液,溶液的pH与NaOH溶液的体积关系如图所示.下列说法错误的是( )
用0.1mol•L-1NaOH溶液滴定10mL0.1mol•L-1H2A溶液,溶液的pH与NaOH溶液的体积关系如图所示.下列说法错误的是( )| A. | A点溶液中加入少量水:$\frac{c(O{H}^{-})}{c({H}_{2}A)}$增大 | |
| B. | B点:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) | |
| C. | C点:c(Na+)=c(HA-)+2c(OH-) | |
| D. | 水电离出来得c(OH-):B>D |
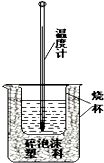 实验室利用如图装置进行中和热的测定.回答下列问题:
实验室利用如图装置进行中和热的测定.回答下列问题: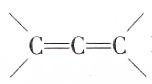 不稳定).
不稳定).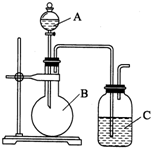 某同学设计如图装置,探究非金属性质变化规律.
某同学设计如图装置,探究非金属性质变化规律.