题目内容
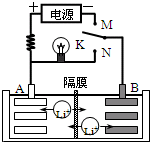 如图是一种可充电的锂离子电池充、放电的工作示意图.放电时该电池的电极反应式为:
如图是一种可充电的锂离子电池充、放电的工作示意图.放电时该电池的电极反应式为:负极:LixC6-xe-═C6+xLi+(LixC6表示锂原子嵌入石墨形成的复合材料)
正极:Li1-xMnO2+xLi++x e-═LiMnO2(LiMnO2表示含锂原子的MnO2)
下列有关说法正确的是( )
A、该电池的反应式为Li1-xMnO2+LixC6
| |||
| B、K与M相接时,A是阳极,发生氧化反应 | |||
| C、K与N相接时,Li+由A极区迁移到B极区 | |||
| D、在整个充电或放电过程中都只存在一种形式的能量转化 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:当K与M相接时,该装置是电解池,A为阳极,阳极上失电子发生氧化反应,B为阴极,发生还原反应,当K与N相接时,该装置是原电池,B为负极,A为正极,负极上发生氧化反应,正极上发生还原反应,原电池放电时,电解质溶液中阳离子向正极移动,阴离子向负极移动.
A.在原电池中,正极和负极反应之和即为电池的总反应;
B.在电解池中,和电源的正极相接的电极是阳极,阳极发生失电子的氧化反应;
C.原电池中,电解质中的阳离子移向正极;
D.存在电能与化学能、热能的转化.
A.在原电池中,正极和负极反应之和即为电池的总反应;
B.在电解池中,和电源的正极相接的电极是阳极,阳极发生失电子的氧化反应;
C.原电池中,电解质中的阳离子移向正极;
D.存在电能与化学能、热能的转化.
解答:
解:当K与M相接时,该装置是电解池,A为阳极,阳极上失电子发生氧化反应,B为阴极,发生还原反应,当K与N相接时,该装置是原电池,B为负极,A为正极,负极上发生氧化反应,正极上发生还原反应,原电池放电时,电解质溶液中阳离子向正极移动,阴离子向负极移动.
A.将正负极电极方程式相加可得Li1-xMnO2+LixC6
LiMnO2+C6,故A错误;
B.K与M相接时,A连接电源的正极,为电解池的是阳极,发生氧化反应,故B正确;
C.K与N相接时,由B的连接方向可知B为负极,原电池工作时,阳离子向正极移动,应向A极移动,故C错误;
D.原电池和电解质中,是电能和化学能之间的相互转化,化学能与热能转化等,故D错误.
故选B.
A.将正负极电极方程式相加可得Li1-xMnO2+LixC6
| 放电 |
| 充电 |
B.K与M相接时,A连接电源的正极,为电解池的是阳极,发生氧化反应,故B正确;
C.K与N相接时,由B的连接方向可知B为负极,原电池工作时,阳离子向正极移动,应向A极移动,故C错误;
D.原电池和电解质中,是电能和化学能之间的相互转化,化学能与热能转化等,故D错误.
故选B.
点评:本题以新型电池为载体考查原电池和电解池原理,明确原电池和电解池电极上得失电子即可解答,注意原电池放电时,阴阳离子的移动方向,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2014年“6?5”世界环境日中国主题为“向污染宣战”.下列行为不利于遏制污染的是( )
| A、发展风能和太阳能等清洁能源,减少使用化石燃料 |
| B、扩建小型钢铁厂、水泥厂,提高钢铁、水泥的产量 |
| C、推广机动车用天然气替代汽、柴油的“油改工程” |
| D、研发可降解的聚碳酸酯替代聚乙烯作一次性塑料袋的生产原料 |
下列说法正确的是( )
| A、科恩和渡普尔因理论化学方面的贡献获得化学界最高成就诺贝尔化学奖,标志着化学已成为以理论研究为主的学科 |
| B、PM2.5表示每立方米空气中直径小于或等于2.5微米的颗粒物的含量,PM2.5值越高,大气污染越严重.因此由PM2.5引起的雾霾一定属于气溶胶 |
| C、对“地沟油”加工处理可以达到变废为宝的目的,比如对“地沟油”进行分馏可以制得汽油、煤油 |
| D、采取“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”等方法,以提高空气质量;推广可利用太阳能、风能等新能源,发展低碳经济,同时能大大减少对环境的污染 |
已知图①~④的相关信息,下列相应叙述正确的是( )


| A、图①表示向恒容密闭容器中充入X和Y发生反应:2X(g)+Y(g)?3Z(g)△H<0,W点X的正反应速率等于M点X的正反应速率 |
| B、图②表示压强对可逆反应A(g)+2B(g)?3C(g)+D(s)的影响,乙的压强比甲的压强小 |
| C、据图③,若要除去CuSO4溶液中的Fe3+,可加入NaOH溶液至PH在4左右 |
| D、常温下,稀释0.1mol/L Na2CO3溶液,图④中的纵坐标可表示溶液中HCO3-的数目 |
下列事实中,能说明氯的非金属性比硫强的是( )
①HClO的氧化性比H2SO4的氧化性强
②常温下氯气是气态而硫是固态
③盐酸酸性比氢硫酸强
④HCl比H2S稳定
⑤H2S能被Cl2氧化成硫
⑥SCl2分子中氯显-1价
⑦氯气与氢气化合比硫与氢气化合要容易进行
⑧Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS.
①HClO的氧化性比H2SO4的氧化性强
②常温下氯气是气态而硫是固态
③盐酸酸性比氢硫酸强
④HCl比H2S稳定
⑤H2S能被Cl2氧化成硫
⑥SCl2分子中氯显-1价
⑦氯气与氢气化合比硫与氢气化合要容易进行
⑧Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS.
| A、①②③④⑤⑥⑦⑧ |
| B、①④⑤⑥⑦ |
| C、④⑤⑥⑦⑧ |
| D、③④⑤⑦⑧ |
X、Y、Z都是金属,把X浸入Z的硝酸盐溶液中,X的表面有Z析出,Z和Y组成原电池时,Z为电池的负极.X、Y、Z三种金属的活动性顺序为( )
| A、X>Y>Z |
| B、X>Z>Y |
| C、Y>X>Z |
| D、Y>Z>X |
某同学按如图所示的装置进行实验,A、B为常见金属,它们的硫酸盐可溶于水.当K闭合时,X电极附近溶液先变红.下列分析不正确的是( )
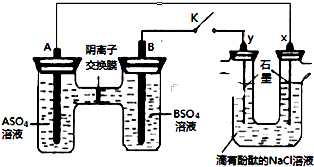

| A、A的金属活动性强于B |
| B、Y的电极反应:2Cl--2e-═Cl2↑ |
| C、阴离子交换膜处的SO42-从左向右移动 |
| D、当电路中有0.1mol电子通过时B电极有0.05mol金属析出 |
化学与科学、技术、社会、环境密切相关,下列有关说法正确的是( )
| A、PM2.5是指大气中直径小于或等于2.5微米的颗粒物,对人体健康或环境有很大影响 |
| B、同位素示踪法、分光光度法、核磁共振技术都是研究化学反应历程的重要手段 |
| C、垃圾焚烧不仅可以用于发电,还不会带来任何新污染 |
| D、地沟油的主要成分是高级脂肪酸甘油酯,故允许加工为食用油,也可用于制肥皂 |