题目内容
17.利用废铅蓄电池的铅泥(PbO、Pb及PbSO4等)可制备精细无机化工产品-3PbO•PbSO4•H2O (三盐),主要制备流程如下: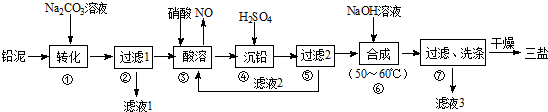
(1)步骤①PbSO4转化为难溶PbCO3的离子方程式为CO32-+PbSO4=PbCO3+SO42-.
(2)滤液1和滤液3经脱色、蒸发、结晶可得到的副产品为Na2SO4•10H2O(或Na2SO4)(写化学式).
(3)步骤③酸溶时,其中的铅与硝酸生成Pb(NO3)2及NO的离子方程式为3Pb+8H++2NO3-=3Pb2++2NO↑+4H2O;滤液2中溶质主要成分为HNO3 (写化学式).
(4)步骤⑥合成三盐的化学方程式为4PbSO4+6NaOH=3Na2SO4+3PbO•PbSO4•H2O+2H2O.
(5)步骤⑦洗涤操作时,检验沉淀是否洗涤完全的方法是取少量最后一次的洗涤过滤液于试管中,向其中滴加盐酸酸化的BaCl2溶液,若不产生白色沉淀,则表明已洗涤完全.
分析 向铅泥中加入Na2CO3溶液,PbSO4转化为难溶PbCO3的离子方程式为CO32-+PbSO4=PbCO3+SO42-,然后过滤得到滤液1为Na2SO4溶液,向滤渣中加入硝酸酸溶,PbO、Pb、PbCO3都与硝酸反应生成Pb(NO3)2,Pb与硝酸反应还生成NO,铅与硝酸生成Pb(NO3)2及NO的离子方程式为3Pb+8H++2NO3-=3Pb2++2NO↑+4H2O,然后向溶液中加入硫酸,生成PbSO4沉淀,过滤,滤液2的主要成分是HNO3,向滤渣中加入NaOH溶液,发生反应4PbSO4+6NaOH=3Na2SO4+3PbO•PbSO4•H2O+2H2O,过滤洗涤干燥得到3PbO•PbSO4•H2O,滤液3中含有Na2SO4,结合题目分析解答.
解答 解:向铅泥中加入Na2CO3溶液,PbSO4转化为难溶PbCO3的离子方程式为CO32-+PbSO4=PbCO3+SO42-,然后过滤得到滤液1为Na2SO4溶液,向滤渣中加入硝酸酸溶,PbO、Pb、PbCO3都与硝酸反应生成 Pb(NO3)2,Pb与硝酸反应还生成NO,铅与硝酸生成Pb(NO3)2及NO的离子方程式为3Pb+8H++2NO3-=3Pb2++2NO↑+4H2O,然后向溶液中加入硫酸,生成PbSO4沉淀,过滤,滤液2的主要成分是HNO3,向滤渣中加入NaOH溶液,发生反应4PbSO4+6NaOH=3Na2SO4+3PbO•PbSO4•H2O+2H2O,过滤洗涤干燥得到3PbO•PbSO4•H2O,滤液3中含有Na2SO4,
(1)通过以上分析知,碳酸钠和硫酸铅发生难溶物的转化,离子方程式为CO32-+PbSO4=PbCO3+SO42-,故答案为:CO32-+PbSO4=PbCO3+SO42-;
(2)通过以上分析知,滤液1和滤液3经脱色、蒸发、结晶可得到的副产品为Na2SO4•10H2O(或Na2SO4),故答案为:Na2SO4•10H2O(或Na2SO4);
(3)通过以上分析知,该离子反应方程式为3Pb+8H++2NO3-=3Pb2++2NO↑+4H2O,滤液2中主要成分是未反应的HNO3,故答案为:3Pb+8H++2NO3-=3Pb2++2NO↑+4H2O;HNO3;
(4)该反应方程式为4PbSO4+6NaOH=3Na2SO4+3PbO•PbSO4•H2O+2H2O,故答案为:4PbSO4+6NaOH=3Na2SO4+3PbO•PbSO4•H2O+2H2O;
(5)该沉淀吸附的离子是硫酸根离子,用盐酸酸化的氯化钡检验,其检验方法为取少量最后一次的洗涤过滤液于试管中,向其中滴加盐酸酸化的BaCl2溶液,若不产生白色沉淀,则表明已洗涤完全,故答案为:取少量最后一次的洗涤过滤液于试管中,向其中滴加盐酸酸化的BaCl2溶液,若不产生白色沉淀,则表明已洗涤完全.
点评 本题考查物质分离和提纯,为高频考点,侧重考查学生分析及知识综合应用能力,涉及基本操作、氧化还原反应、离子反应等知识点,明确流程图中发生的反应或操作方法是解本题关键,注意基础知识的积累和灵活运用,题目难度中等.

 导学全程练创优训练系列答案
导学全程练创优训练系列答案 某有机物的结构简式如下所示,则下列关于该有机化合物的各项叙述正确的是( )
某有机物的结构简式如下所示,则下列关于该有机化合物的各项叙述正确的是( )| A. | 该有机物遇氯化铁溶液不呈紫色 | |
| B. | 1mol该有机物能与6mol氢氧化钠反应 | |
| C. | 该有机物能与6mol金属钠反应生成6molH2 | |
| D. | 在稀硫酸存在下可以发生水解反应,但水解的产物只有一种有机物 |
| A. | 增大压强可提高反应速率 | |
| B. | 升高温度可减小反应速率 | |
| C. | 若反应物的总能量比生成物的总能量低,说明该反应是放热反应 | |
| D. | 增大氧气的浓度可使NO2转化率为100% |
①
 ②乙烯③SO2 ④氯乙烯
②乙烯③SO2 ④氯乙烯⑤CH2═CH-COOH ⑥苯 ⑦聚乙烯.
| A. | ①⑥⑦ | B. | ①③④⑥ | C. | ①④⑦ | D. | ①③⑥⑦ |
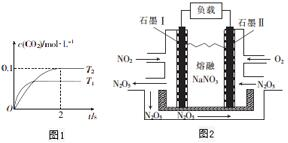 汽车尾气和燃煤尾气是造成空气污染的原因之一.
汽车尾气和燃煤尾气是造成空气污染的原因之一.