题目内容
液氨常用作制冷剂,回答下列问题
(1)一定条件下在密闭容器中发生反应:
a.NH4I(s)?NH3(g)+HI(g) b.2HI(g)?H2(g)+I2(g)
①写出反应a的平衡常数表达式
②达到平衡后,扩大容器体积,反应b的移动方向 (填“正向”、“逆向”或“不移动”),达到新的平衡时容器内颜色将怎样变化 (填“加深”、“变浅”或“不变”)
(2)工业上合成氨的反应:N2(g)+3H2(g)?2NH3(g)△H=-92.60kJ?mol-1
下列说法能说明上述反应向正反应方向进行的是 (填序号).
a.单位时间内生成2n mol NH3的同时生成3n mol H2
b.单位时间内生成6n mol N-H键的同时生成2n mol H-H键
c.用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1:3:2
d.混合气体的平均摩尔质量增大
e.容器内的气体密度不变
(3)已知合成氨反应在某温度下2L的密闭容器中进行,测得如下数据:
根据表中数据计算:
①反应进行到2h时放出的热量为 kJ.
②0~1h内N2的平均反应速率为 mol?L-1?h-1.
③此温度下该反应的化学平衡常数K= (保留两位小数).
④反应达到平衡后,若往平衡体系中再加入N2、H2和NH3各1.00mol,化学平衡将向 方向移动(填“正反应”或“逆反应”).
(4)肼(N2H4)的性质类似于NH3,极易溶于水,与水反应生成一种二元弱碱在溶液中分步电离,请用离子反应方程式表示其水溶液显碱性的原因 .
(1)一定条件下在密闭容器中发生反应:
a.NH4I(s)?NH3(g)+HI(g) b.2HI(g)?H2(g)+I2(g)
①写出反应a的平衡常数表达式
②达到平衡后,扩大容器体积,反应b的移动方向
(2)工业上合成氨的反应:N2(g)+3H2(g)?2NH3(g)△H=-92.60kJ?mol-1
下列说法能说明上述反应向正反应方向进行的是
a.单位时间内生成2n mol NH3的同时生成3n mol H2
b.单位时间内生成6n mol N-H键的同时生成2n mol H-H键
c.用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1:3:2
d.混合气体的平均摩尔质量增大
e.容器内的气体密度不变
(3)已知合成氨反应在某温度下2L的密闭容器中进行,测得如下数据:
时间(h) 物质的量(mol) | 0 | 1 | 2 | 3 | 4 |
| N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
| NH3 | 0 | 0.20 | n2 | 1.00 | 1.00 |
①反应进行到2h时放出的热量为
②0~1h内N2的平均反应速率为
③此温度下该反应的化学平衡常数K=
④反应达到平衡后,若往平衡体系中再加入N2、H2和NH3各1.00mol,化学平衡将向
(4)肼(N2H4)的性质类似于NH3,极易溶于水,与水反应生成一种二元弱碱在溶液中分步电离,请用离子反应方程式表示其水溶液显碱性的原因
考点:化学平衡的计算,反应速率的定量表示方法,化学平衡建立的过程,化学平衡的影响因素
专题:
分析:(1)①化学平衡常数K=[NH3][HI];
②减小压强,平衡向气体体积增大的方向移动;
(2)a.单位时间内生成2n molNH3的同时生成3n molH2,该反应达到平衡状态;
b.单位时间内生成6nmolN-H键时消耗3nmolH-H键,实际上同时生成2n molH-H键,则v(正)>v(逆);
c.用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1:3:2,该反应不一定向正反应方向移动;
d.混合气体的平均摩尔质量增大,混合气体的质量不变,则混合气体的物质的量减小,平衡向气体体积减小的方向移动;
e.容器内的气体密度始终不变;
(3)①根据氮气和反应热之间的关系式计算;
②先计算正确的平均反应速率,再根据同一可逆反应中,同一时间段内各物质的反应速率之比等于其计量数之比计算氮气反应速率;
③2h时,△n(N2)=(1.50-1.20)mol=0.30mol,根据N2---2NH3之间的关系式得△n(NH3)=2△n(N2)=0.60mol,3h和4h时,各物质的物质的量不变,则该反应达到平衡状态,化学平衡常数K=
;
④根据浓度商和平衡常数相对大小判断反应方向;
(4)根据一水合氨电离方式书写N2H4?2H2O电离方程式.
②减小压强,平衡向气体体积增大的方向移动;
(2)a.单位时间内生成2n molNH3的同时生成3n molH2,该反应达到平衡状态;
b.单位时间内生成6nmolN-H键时消耗3nmolH-H键,实际上同时生成2n molH-H键,则v(正)>v(逆);
c.用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1:3:2,该反应不一定向正反应方向移动;
d.混合气体的平均摩尔质量增大,混合气体的质量不变,则混合气体的物质的量减小,平衡向气体体积减小的方向移动;
e.容器内的气体密度始终不变;
(3)①根据氮气和反应热之间的关系式计算;
②先计算正确的平均反应速率,再根据同一可逆反应中,同一时间段内各物质的反应速率之比等于其计量数之比计算氮气反应速率;
③2h时,△n(N2)=(1.50-1.20)mol=0.30mol,根据N2---2NH3之间的关系式得△n(NH3)=2△n(N2)=0.60mol,3h和4h时,各物质的物质的量不变,则该反应达到平衡状态,化学平衡常数K=
| c 2(NH 3) |
| c(N 2).c 3(H 2) |
④根据浓度商和平衡常数相对大小判断反应方向;
(4)根据一水合氨电离方式书写N2H4?2H2O电离方程式.
解答:
解:(1)①化学平衡常数K=[NH3][HI],故答案为:K=[NH3][HI];
②方程式a是反应前后气体体积增大的反应,b方程式反应前后气体体积不变,所以增大容器体积,压强减小,平衡向气体体积增大的方向移动,所以平衡向正反应方向移动,因为容器体积增大,平衡时气体颜色变浅,故答案为:正向;变浅;
(2)a.单位时间内生成2nmolNH3的同时消耗3nmolH2,同时生成3n molH2,则氢气的正逆反应速率相等,所以该反应达到平衡状态,故错误;
b.单位时间内生成6nmolN-H键时消耗3nmolH-H键,实际上同时生成2n molH-H键,则v(正)>v(逆),则平衡向在反应方向移动,故正确;
c.用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1:3:2,无论该反应是否达到平衡状态都存在反应速率之比为1:3:2,所以不能确定该反应向正反应方向移动,故错误;
d.混合气体质量不变,如果混合气体的平均摩尔质量增大,则平衡向气体体积减小的正反应方向移动,故正确;
e.混合气体质量不变,容器体积不变,所以容器内的气体密度始终不变,故错误;
故选:bd;
(3)①该反应有1mol氮气参加反应放出92.60kJ热量,则生成(1.50-1.20)mol氮气参加反应放出的热量=
=27.78kJ,故答案为:27.78;
②2h内,v(NH3)=
=0.1mol/(L.h),同一可逆反应中,同一时间段内各物质的反应速率之比等于其计量数之比,所以v(N2)=
v(NH3)=0.05mol/(L.h),
故答案为:0.05;
③2h时,△n(N2)=(1.50-1.20)mol=0.30mol,根据N2---2NH3之间的关系式得△n(NH3)=2△n(N2)=0.60mol,3h和4h时,各物质的物质的量不变,则该反应达到平衡状态,c(NH3)=
=0.5mol/L,c(N2)
=
=0.5mol/L,c(H2)=
=1.5mol/L,
化学平衡常数K=
=
=0.15,
故答案为:0.15;
④再加入N2、H2和NH3各1.00mol,c(NH3)=1mol/L,c(N2)=1mol/L,c(H2)=2mol/L,
浓度商=
=0.125<K,则平衡向正反应方向移动,故答案为:正反应;
(4)肼(N2H4)的性质类似于NH3,极易溶于水,与水反应生成一种二元弱碱N2H4?2H2O,该二元弱碱电离,电离方程式为:N2H4?2H2O?[N2H5?H2O]++OH-,
故答案为:N2H4?2H2O?[N2H5?H2O]++OH-.
②方程式a是反应前后气体体积增大的反应,b方程式反应前后气体体积不变,所以增大容器体积,压强减小,平衡向气体体积增大的方向移动,所以平衡向正反应方向移动,因为容器体积增大,平衡时气体颜色变浅,故答案为:正向;变浅;
(2)a.单位时间内生成2nmolNH3的同时消耗3nmolH2,同时生成3n molH2,则氢气的正逆反应速率相等,所以该反应达到平衡状态,故错误;
b.单位时间内生成6nmolN-H键时消耗3nmolH-H键,实际上同时生成2n molH-H键,则v(正)>v(逆),则平衡向在反应方向移动,故正确;
c.用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1:3:2,无论该反应是否达到平衡状态都存在反应速率之比为1:3:2,所以不能确定该反应向正反应方向移动,故错误;
d.混合气体质量不变,如果混合气体的平均摩尔质量增大,则平衡向气体体积减小的正反应方向移动,故正确;
e.混合气体质量不变,容器体积不变,所以容器内的气体密度始终不变,故错误;
故选:bd;
(3)①该反应有1mol氮气参加反应放出92.60kJ热量,则生成(1.50-1.20)mol氮气参加反应放出的热量=
| 92.60kJ |
| 1mol |
②2h内,v(NH3)=
| ||
| 1h |
| 1 |
| 2 |
故答案为:0.05;
③2h时,△n(N2)=(1.50-1.20)mol=0.30mol,根据N2---2NH3之间的关系式得△n(NH3)=2△n(N2)=0.60mol,3h和4h时,各物质的物质的量不变,则该反应达到平衡状态,c(NH3)=
| 1.00mol |
| 2L |
=
| 1.00mol |
| 2L |
| 3mol |
| 2L |
化学平衡常数K=
| c 2(NH 3) |
| c(N 2).c 3(H 2) |
| 0.5×0.5 |
| 0.5×(1.5) 3 |
故答案为:0.15;
④再加入N2、H2和NH3各1.00mol,c(NH3)=1mol/L,c(N2)=1mol/L,c(H2)=2mol/L,
浓度商=
| 1×1 |
| 1×2 3 |
(4)肼(N2H4)的性质类似于NH3,极易溶于水,与水反应生成一种二元弱碱N2H4?2H2O,该二元弱碱电离,电离方程式为:N2H4?2H2O?[N2H5?H2O]++OH-,
故答案为:N2H4?2H2O?[N2H5?H2O]++OH-.
点评:本题考查了化学平衡的有关知识,涉及化学平衡常数的有关计算、化学平衡状态的判断、化学反应速率的计算等知识点,根据平衡常数公式、正逆反应速率相等、化学反应速率公式进行分析解答即可,注意化学平衡状态的判断中,只有反应前后改变的物理量,才能作为化学平衡状态的判断依据,题目难度中等.

练习册系列答案
相关题目
在温度、容积相同的3个密闭容器中,按下表投入反应物.发生反应:H2(g)+I2(g)═2HI(g)△H=14.9kJ?mol-1,在恒温、恒容条件下,测得反应达到平衡时的有关数据如下:
下列说法正确的是( )
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol H2 1mol I2 | 2mol HI | 4mol HI |
| HI的浓度 | c1 | c2 | c3 |
| 反应的能量变化 | 放出akg | 吸收bkg | 吸收ckg |
| 反应物转化率 | α1 | α2 | α3 |
| A、2α1=α3 |
| B、α1+α2=1 |
| C、c1=c2=c3 |
| D、a+b=14.9 |
往下列溶液中,通入足量CO2气体,最终能产生白色沉淀的是( )
| A、饱和Na2CO3溶液 |
| B、澄清石灰水 |
| C、CaCl2溶液 |
| D、盐酸 |
向一定量的Fe、FeO、Fe2O3的混合物中加入100mL浓度为1.0mol?L-1的盐酸,恰好使混合物完全溶解,有气体放出,所得溶液中加入KSCN溶液后无血红色出现.若用足量的CO在高温下还原相同质量此混合物,能得到铁的质量是( )
| A、11.2g | B、5.6g |
| C、2.8g | D、1.4g |
糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质.以下叙述正确的是( )
| A、植物油不能使溴的四氯化碳溶液褪色 |
| B、淀粉和纤维素都可以作为工业上生产葡萄糖的原料 |
| C、糖类、油脂、蛋白质在一定条件下都能发生水解反应 |
| D、蛋白质溶液遇硫酸铜后产生的沉淀能重新溶于水 |

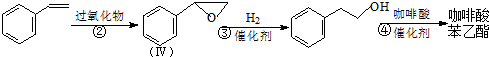
 的芳香化合物共有5种
的芳香化合物共有5种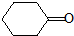 )与化合物Ⅱ也能发生反应①的反应,则其生成含羧基的化合物的结构简式为
)与化合物Ⅱ也能发生反应①的反应,则其生成含羧基的化合物的结构简式为
 甲醇是主要的化学工业基础原料和清洁液体燃料.工业上可以用CO或CO2来生产燃料甲醇.已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
甲醇是主要的化学工业基础原料和清洁液体燃料.工业上可以用CO或CO2来生产燃料甲醇.已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示: