题目内容
 甲醇是主要的化学工业基础原料和清洁液体燃料.工业上可以用CO或CO2来生产燃料甲醇.已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
甲醇是主要的化学工业基础原料和清洁液体燃料.工业上可以用CO或CO2来生产燃料甲醇.已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:| 化学反应及平衡常数 | 温度/℃ | ||
| 500 | 800 | ||
| ①2H2(g)+CO(g)?CH3OH(g)△H1 | K1 | 2.5 | 0.15 |
| ②H2(g)+CO2(g)?CO(g)+H2O(g)△H2 | K2 | 1.0 | 2.50 |
| ③3H2(g)+CO2(g)?CH3OH(g)+H2O(g)△H3 | K3 | ||
(2)某温度下反应①中H2的平衡转化率(a)与体系总压强(P)的关系如图1所示.则平衡状态由A变到B时,平衡常数K(A)
(3)根据反应①与②可推导出K1、K2与K3之间的关系,则K3=
(4)在3L容积可变的密闭容器中发生反应②,已知c(CO)与反应时间t变化曲线Ⅰ如图2所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ.当曲线Ⅰ变为曲线Ⅱ时,改变的条件是
(5)一定条件下甲醇与一氧化碳反应可以合成乙酸.通常状况下,将amol/L的乙酸与bmol/LBa(OH)2溶液等体积混合,反应平衡时,2c(Ba2+)=c(CH3COO-),用含a和b的代数式表示该混合溶液中乙酸的电离常数为
考点:化学平衡常数的含义
专题:化学平衡专题
分析:(1)分析图表数据,反应②平衡常数随温度升高增大,平衡正向进行,正反应是吸热反应;
(2)依据平衡常数随温度变化,不随压强变化分析;
(3)反应③是气体体积减小的反应△S<0,分析反应特征可知平衡常数K3=K1×K2,计算不同温度下反应③的平衡常数,结合温度变化分析判断反应焓变△H<0,依据反应①+②得到反应③,所以平衡常数K3=K1×K2;依据某时刻浓度商计算和平衡常数比较判断反应进行的方向;
(4)图象分析曲线Ⅰ变化为曲线Ⅱ是缩短反应达到平衡的时间,最后达到相同平衡状态,体积是可变得是恒压容器,说明改变的是加入了催化剂;当曲线Ⅰ变为曲线Ⅲ时一氧化碳物质的量增大,反应是气体体积不变的反应,可变容器中气体体积和浓度成反比,气体物质的量不变;
(5)溶液等体积混合溶质浓度减少一半,醋酸电离平衡常数与浓度无关,结合概念计算.
(2)依据平衡常数随温度变化,不随压强变化分析;
(3)反应③是气体体积减小的反应△S<0,分析反应特征可知平衡常数K3=K1×K2,计算不同温度下反应③的平衡常数,结合温度变化分析判断反应焓变△H<0,依据反应①+②得到反应③,所以平衡常数K3=K1×K2;依据某时刻浓度商计算和平衡常数比较判断反应进行的方向;
(4)图象分析曲线Ⅰ变化为曲线Ⅱ是缩短反应达到平衡的时间,最后达到相同平衡状态,体积是可变得是恒压容器,说明改变的是加入了催化剂;当曲线Ⅰ变为曲线Ⅲ时一氧化碳物质的量增大,反应是气体体积不变的反应,可变容器中气体体积和浓度成反比,气体物质的量不变;
(5)溶液等体积混合溶质浓度减少一半,醋酸电离平衡常数与浓度无关,结合概念计算.
解答:
解:(1)分析图表数据,反应②平衡常数随温度升高增大,平衡正向进行,正反应是吸热反应,故答案为:>;
(2)依据平衡常数随温度变化,不随压强变化分析,图象中平衡状态由A变到B时,压强改变,温度不变,所以平衡常数不变,故答案为:=;
(3)反应③3H2(g)+CO2(g)═CH3OH(g)+H2O(g)是气体体积减小的反应△S<0,依据反应①+②得到反应③,所以平衡常数K3=K1×K2;计算不同温度下反应③的平衡常数,500°C时,K3=K1×K2=2.5×1.0=2.5,800°C时,K3=K1×K2=2.5×0.15=0.375,结合温度变化分析,随温度升高,平衡常数减小,平衡逆向进行,所以判断反应是放热反应,焓变△H<0,在500℃、2L的密闭容器中,进行反应③,测得反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O (g)的浓度(mol/L)分别为0.8、0.1、0.3、0.15,Q=
=0.87<K=2.5,反应正向进行,V正>V逆,
故答案为:K1?K2;>;
(4)图象分析曲线Ⅰ变化为曲线Ⅱ是缩短反应达到平衡的时间,最后达到相同平衡状态,体积是可变得是恒压容器,说明改变的是加入了催化剂;当曲线Ⅰ变为曲线Ⅲ时一氧化碳物质的量增大,反应是气体体积不变的反应,可变容器中气体体积和浓度成反比,气体物质的量不变,曲线Ⅰ,体积为3L,一氧化碳浓度为3mol/L,改变条件不好为曲线Ⅱ,一氧化碳浓度为4.5mol/L,则体积压缩体积为:3:V=4.5:3,V=2L,所以将容器的体积快速压缩至2L符合;
故答案为:加入催化剂;将容器的体积快速压缩至2L;
(5)通常状况下,将a mol/L的醋酸与b mol/L Ba(OH)2溶液等体积混合,溶液中溶质为醋酸钡和氢氧化钡,反应平衡时,2c(Ba2+)=c(CH3COO-)=bmol/L,溶液中c(H+)=c(OH-)=10-7mol/L,溶液呈中性,醋酸电离平衡常数依据电离方程式写出K=
=
=
×10-7L/mol;
故答案为:
×10-7L/mol.
(2)依据平衡常数随温度变化,不随压强变化分析,图象中平衡状态由A变到B时,压强改变,温度不变,所以平衡常数不变,故答案为:=;
(3)反应③3H2(g)+CO2(g)═CH3OH(g)+H2O(g)是气体体积减小的反应△S<0,依据反应①+②得到反应③,所以平衡常数K3=K1×K2;计算不同温度下反应③的平衡常数,500°C时,K3=K1×K2=2.5×1.0=2.5,800°C时,K3=K1×K2=2.5×0.15=0.375,结合温度变化分析,随温度升高,平衡常数减小,平衡逆向进行,所以判断反应是放热反应,焓变△H<0,在500℃、2L的密闭容器中,进行反应③,测得反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O (g)的浓度(mol/L)分别为0.8、0.1、0.3、0.15,Q=
| 0.15×0.3 |
| 0.83×0.1 |
故答案为:K1?K2;>;
(4)图象分析曲线Ⅰ变化为曲线Ⅱ是缩短反应达到平衡的时间,最后达到相同平衡状态,体积是可变得是恒压容器,说明改变的是加入了催化剂;当曲线Ⅰ变为曲线Ⅲ时一氧化碳物质的量增大,反应是气体体积不变的反应,可变容器中气体体积和浓度成反比,气体物质的量不变,曲线Ⅰ,体积为3L,一氧化碳浓度为3mol/L,改变条件不好为曲线Ⅱ,一氧化碳浓度为4.5mol/L,则体积压缩体积为:3:V=4.5:3,V=2L,所以将容器的体积快速压缩至2L符合;
故答案为:加入催化剂;将容器的体积快速压缩至2L;
(5)通常状况下,将a mol/L的醋酸与b mol/L Ba(OH)2溶液等体积混合,溶液中溶质为醋酸钡和氢氧化钡,反应平衡时,2c(Ba2+)=c(CH3COO-)=bmol/L,溶液中c(H+)=c(OH-)=10-7mol/L,溶液呈中性,醋酸电离平衡常数依据电离方程式写出K=
| c(CH3COO-)c(H+) |
| c(CH3COOH) |
| b×10-7 | ||
|
| 2b |
| a-2b |
故答案为:
| 2b |
| a-2b |
点评:本题考查了化学平衡影响因素分析判断,平衡常数计算和影响条件的应用,难溶电解质溶液中溶度积的计算,题目综合性较大.

练习册系列答案
 名题金卷系列答案
名题金卷系列答案 优加精卷系列答案
优加精卷系列答案
相关题目
我国自主研发的新一代动车组在京沪高铁上跑出过486.1公里的世界列车最高时速,这得益于全路铺设的优质无缝平滑的超长钢轨.下列有关说法不正确的是( )
| A、制造钢轨的材料是钢,钢是用量最大的合金 |
| B、钢的熔点比铁的熔点高,而铁的用途更广泛 |
| C、我国在商代就开始使用铜合金 |
| D、铝合金的强度、硬度比组成合金各成分金属的大 |
下列叙述正确的是( )
| A、合成氨工业中,移走NH3可增大正反应速率,提高原料转化率 |
| B、酸碱中和滴定时,锥形瓶需用待测液润洗2次,再加入待测液 |
| C、将NO2、N2O4混合气体的体积压缩为原来的一半,则气体颜色加深 |
| D、牺牲阳极的阴极保护法和外加直流电源的阴极保护法都是应用电解原理 |
下列有关阿伏加德罗常数NA的说法中,不正确的是( )
| A、标准状况下,分子数为NA的N2、C2H4混合气体的总质量为28g |
| B、0.1mol Mg在空气中完全燃烧生成MgO和Mg3N2,转移的电子数目为0.2NA |
| C、60gCaCO3与KHCO3的混合物与足量盐酸反应生成CO2分子数为0.6NA |
| D、常温常压下,将0.1mol氯气通入水中发生化学反应,转移电子数为0.1NA |
关于钠的叙述中,正确的是( )
| A、钠是银白色金属,硬度很大 |
| B、将金属钠放在石棉网上用酒精灯加热后,金属钠剧烈燃烧,产生黄色火焰,生成Na2O2 |
| C、金属钠在空气中燃烧,生成氧化钠 |
| D、金属钠的熔点很高 |
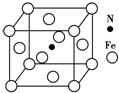 铁及其化合物在有机化学中应用广泛,例如有机合成中,常用铁和盐酸将硝基(-NO2)还原为氨基(-NH2);在苯的溴代反应中用溴化铁作催化剂.
铁及其化合物在有机化学中应用广泛,例如有机合成中,常用铁和盐酸将硝基(-NO2)还原为氨基(-NH2);在苯的溴代反应中用溴化铁作催化剂.