题目内容
13.现有一组溶液:①汽油和氯化钠溶液;②39%的乙醇溶液;③氯化钠和单质碘的水溶液,分离以上各混合液的正确方法依次是( )| A. | 分液 蒸馏 萃取 | B. | 萃取 蒸馏 分液 | C. | 分液 萃取 蒸馏 | D. | 蒸馏 萃取 分液 |
分析 ①汽油和氯化钠溶液,混合分层;②39%的乙醇溶液中乙醇与水的沸点不同,③单质碘不易溶于水,易溶于有机溶剂,以此来解答.
解答 解:①汽油和氯化钠溶液不相溶,汽油的密度比水的小,所以在上层,可通过分液的方法进行分离;
②乙醇和水的沸点不同,可通过蒸馏的方法进行分离;
③碘在水溶液中的溶解度不大,可用有机溶剂把它从其水溶液中萃取出来.
故选A.
点评 本题考查混合物分离、提纯的方法及选择,为高频考点,把握物质的性质及性质差异、混合物分离方法为解答的关键,注重实验基础知识和基本技能的考查,注意有机物性质,题目难度不大.

练习册系列答案
相关题目
3.根据教材中提供的制硝基苯的反应: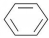 +HNO3(浓)$\frac{\underline{\;\;\;浓硫酸\;\;\;}}{50~60℃}$
+HNO3(浓)$\frac{\underline{\;\;\;浓硫酸\;\;\;}}{50~60℃}$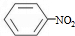 +H2O设计一个实验制取一定量的纯净硝基苯.有关信息见下表:
+H2O设计一个实验制取一定量的纯净硝基苯.有关信息见下表:
可供选择的实验用品:
①仪器:烧杯、大试管、铁架台(带铁夹和铁圈)、石棉网、酒精灯、橡胶塞、玻璃管、温度计、分液漏斗、蒸馏烧瓶、冷凝管、牛角管、锥形瓶等.
②药品:浓硝酸、稀硝酸、浓硫酸、稀硫酸、苯、5%NaOH溶液、无水氯化钙、蒸馏水等.
第一步:选择合适的实验仪器及条件.
(1)请补充完整下列制取硝基苯的装置图(要求注明所画出玻璃仪器名称).

(2)为了防止反应过程中有毒物质挥发到空气中,本装置中使用了长玻璃导管(填仪器名称).所起到的作用是冷凝回流.
第二步:安排合理的实验步骤.
(3)连接装置,检查装置气密性,加入药品,加热反应至实验完成.
第三步:产品提纯.根据上述提供仪器及药品设计实验得到纯净干燥的硝基苯.
(4)简要写出下列各步操作:
问题分析:
(5)纯净的硝基苯是一种有苦杏仁味的无色液体,而实验中得到的产品往往呈淡黄色,可能的原因是含有少量硝酸分解产生的二氧化氮.
 +HNO3(浓)$\frac{\underline{\;\;\;浓硫酸\;\;\;}}{50~60℃}$
+HNO3(浓)$\frac{\underline{\;\;\;浓硫酸\;\;\;}}{50~60℃}$ +H2O设计一个实验制取一定量的纯净硝基苯.有关信息见下表:
+H2O设计一个实验制取一定量的纯净硝基苯.有关信息见下表:| 物质 | 熔点/℃ | 沸点/℃ | 相对密度/(20℃) | 毒性 | 水溶性 |
| 苯 | 5.5 | 80.1 | 0.8794 | 有 | 不溶于水 |
| 硝酸 | -41.59 | 83 | 1.503 | - | 易溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 有 | 不溶于水 |
| 硫酸 | 10.0 | 338 | 1.84 | - | 易溶于水 |
①仪器:烧杯、大试管、铁架台(带铁夹和铁圈)、石棉网、酒精灯、橡胶塞、玻璃管、温度计、分液漏斗、蒸馏烧瓶、冷凝管、牛角管、锥形瓶等.
②药品:浓硝酸、稀硝酸、浓硫酸、稀硫酸、苯、5%NaOH溶液、无水氯化钙、蒸馏水等.
第一步:选择合适的实验仪器及条件.
(1)请补充完整下列制取硝基苯的装置图(要求注明所画出玻璃仪器名称).

(2)为了防止反应过程中有毒物质挥发到空气中,本装置中使用了长玻璃导管(填仪器名称).所起到的作用是冷凝回流.
第二步:安排合理的实验步骤.
(3)连接装置,检查装置气密性,加入药品,加热反应至实验完成.
第三步:产品提纯.根据上述提供仪器及药品设计实验得到纯净干燥的硝基苯.
(4)简要写出下列各步操作:
| 1 | 用蒸馏水洗涤反应混合液,分液后取下层液体 |
| 2 | |
| 3 | |
| 4 | |
| 5 |
(5)纯净的硝基苯是一种有苦杏仁味的无色液体,而实验中得到的产品往往呈淡黄色,可能的原因是含有少量硝酸分解产生的二氧化氮.
1.短周期元素X、Y、Z、W、Q在元素周期表中的位置如表所示,其中X元素的原子内层电子数是最外层电子数的一半,则下列说法中不正确的是( )
| X | Y | ||
| Z | W | Q |
| A. | 由Y与W形成的氧化物溶于水一定是强酸 | |
| B. | Z和Y组成的物质是原子晶体 | |
| C. | Z与Q形成的物质能与H2在一定条件下反应 | |
| D. | X和Y均存在同素异形体 |
8.下列检验Fe3+的方法错误的是( )
| A. | 加入NaOH溶液,生成灰白色沉淀迅速变成灰绿色,最后变成红褐色 | |
| B. | 加入NaOH溶液,生成红褐色沉淀 | |
| C. | 加入硫氰化钾溶液,显示红色 | |
| D. | 加入氨水,生成红褐色沉淀 |
5.如图是利用二氧化硅是制备硅及其化合物的流程,下列说法正确的是( )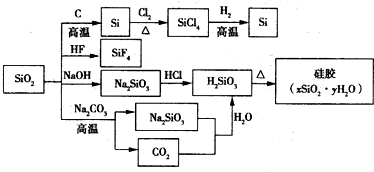

| A. | SiO2属于两性氧化物 | |
| B. | 盛放Na2CO3溶液的试剂瓶不能用玻璃塞 | |
| C. | 硅胶吸水后可重复再生 | |
| D. | 图中所示转化反应都是氧化还原反应 |
2.有200mL氯化镁和氯化铝的混合溶液,其中c(Mg2+)为0.2mol?L-1,c(Cl-)为1.3mol?L-1.要使Mg2+全部转化为沉淀分离出来,至少需加4mol?L-1NaOH溶液的体积为( )
| A. | 40mL | B. | 72mL | C. | 80mL | D. | 128mL |
3.下列关于氯气的叙述正确的是( )
| A. | 氢气在氯气中燃烧产生苍白色火焰 | |
| B. | 铁丝在氯气中燃烧生成FeCl2 | |
| C. | 氯气的水溶液用于漂白,是利用氯气的强氧化性 | |
| D. | 当有大量氯气逸到空气中时,可用浸有NaOH溶液的毛巾捂住鼻子 |