题目内容
1.下列反应的离子方程式书写正确的是( )| A. | 硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液:Fe2++2H++H2O2═Fe3++2H2O | |
| B. | 已知同温度下的溶解度:Zn(OH)2>ZnS,Na2S溶液与ZnCl2溶液混合:Zn2++S2-+2H2O═Zn(OH)2↓+H2S↑ | |
| C. | 0.01 mol•L-1NH4Al(SO4)2溶液与0.02 mol•L-1 Ba(OH)2溶液等体积混合:Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O | |
| D. | 向KI-淀粉溶液中加入稀硫酸,在空气中放置一段时间后,溶液呈蓝色:4H++4I-+O2═2I2+2H2O |
分析 A.发生氧化还原反应生成硫酸铁和水,选项反应方程式反应前后的电荷不守恒;
B.Zn2++S2-+2H2O═Zn(OH)2↓+H2S↑表示Zn2+、S2-+双水解,不是溶解度:Zn(OH)2>ZnS原因;
C.二者反应生成硫酸钡、氢氧化铝和一水合氨;
D.由现象可知,碘离子被氧气氧化生成碘单质.
解答 解:A.硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液,反应前后的电荷不守恒,正确的离子方程式为:2Fe2++H2O2+2H+═2Fe3++2H2O,故A错误;
B.同温度下的溶解度:Zn(OH)2>ZnS,因ZnS比Zn(OH)2难溶,S2-和Zn2+应先结合成ZnS沉淀,而不是Zn2++S2-+2H2O═Zn(OH)2↓+H2S↑双水解,故B错误;
C.0.01 mol•L-1NH4Al(SO4)2溶液与0.02 mol•L-1 Ba(OH)2溶液等体积混合:生成硫酸钡、氢氧化铝和一水合氨,离子方程式:NH4++Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+Al(OH)3↓+NH3•H2O,故C错误;
D.由现象可知,碘离子被氧化生成碘单质,离子反应为4H++4I-+O2═2I2+2H2O,故D正确;
故选D.
点评 本题考查离子反应的书写,明确发生的化学反应是解答本题的关键,注意C选项与量有关的离子反应是解答的难点,题目难度中等.

练习册系列答案
相关题目
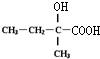
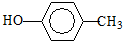
12.由2个一CH3,3个-CH2-、1个 、1个-OH构成的有机物的数目为( )
、1个-OH构成的有机物的数目为( )
 、1个-OH构成的有机物的数目为( )
、1个-OH构成的有机物的数目为( )| A. | 4 | B. | 5 | C. | 6 | D. | 7 |
16.化学与人类社会生产、生活密切相关,下列说法正确的是( )
| A. | 误食重金属盐引起人体中毒,可喝大量的食盐水解毒 | |
| B. | 光纤通信使用的光缆主要成分是Si,太阳能电池使用的材料主要是SiO2 | |
| C. | 陶瓷、砖瓦、玻璃、水泥等,都是硅酸盐产品 | |
| D. | 钢铁制品和铜制品既能发生吸氧腐蚀又能发生析氢腐蚀 |
6.化学与人类生产、生活、社会可持续发展密切相关,下列说法不正确的是( )
| A. | 在羽毛球、网球等体育项目中做球拍的碳纤维材料是一种新型无机非金属材料 | |
| B. | 从海水中提取溴和镁都必须通过化学反应才能实现 | |
| C. | 聚乙烯塑料的老化是由于发生了加成反应 | |
| D. | 用饱和NH4Cl溶液可除去铁表面的锈斑 |
13.化学与人类生活密切相关,下列与化学有关的说法正确的是( )
| A. | 贮氢金属并不是简单地吸附氢气,而是通过化学反应贮存氢气 | |
| B. | 光分解水制氢气、植物秸秆制沼气、高粱制乙醇都涉及生物质能的利用 | |
| C. | 煤的主要成分为单质碳、苯、二甲苯等,因而可通过煤的干馏将它们分离 | |
| D. | 化学药品着火,都要立即用水或泡沫灭火器灭火 |
10.下列有关实验的操作、现象和结论或解释 都正确的是( )
| 选项 | 操作 | 现象 | 结论或解释 |
| A | 用pH计或pH试纸分别测定饱和SO2水溶液和饱和CO2水溶液的pH值 | 饱和SO2水溶液的pH值小于饱和CO2水溶液 | 亚硫酸强于碳酸 |
| B | 向加热KClO3制氧气后的残余固体中加入浓H2SO4,继续加热 | 产生黄绿色气体 | 浓硫酸与残渣中的KCl发生反应生成了Cl2 |
| C | 加热装在试管中的NH4Cl晶体 | 试管底部的晶体消失,试管上部有晶体凝结. | NH4Cl晶体发生了升华. |
| D | 将一根较粗的铜丝在酒精灯火焰上加热到红热,然后趁热插入乙醇中一会儿取出. | 铜丝先变黑后又变红,乙醇中伴有刺激性气味产生. | 铜丝发生了几个反应,但铜丝前后的质量不变. |
| A. | A | B. | B | C. | C | D. | D |
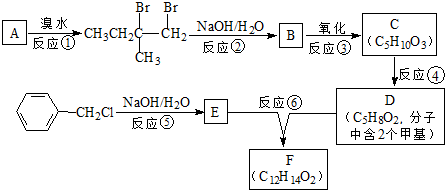
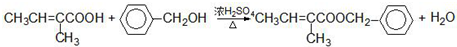 .
. :
: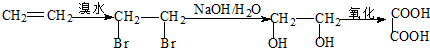 .
.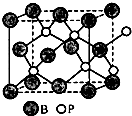 X、Y、Z、W、A五种元素,均位于周期表的前四周期,它们的核电荷数依次增加,且核电荷数之和为57.Y原子的L层p轨道中有2个电子,Z的原子核外有三个未成对电子,W与Y原子的价电子数相同,A原子的最外层电子数是最内层电子数的一半,其d轨道处于全充满状态.
X、Y、Z、W、A五种元素,均位于周期表的前四周期,它们的核电荷数依次增加,且核电荷数之和为57.Y原子的L层p轨道中有2个电子,Z的原子核外有三个未成对电子,W与Y原子的价电子数相同,A原子的最外层电子数是最内层电子数的一半,其d轨道处于全充满状态.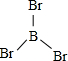 .
.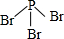 .
.