题目内容
11.某烧碱样品中含有少量不与酸作用的可溶性杂质,为了测定其纯度,进行以下滴定操作:A.转移到容量瓶中最终配制成250mL烧碱溶液;
B.用移液管(或碱式滴定管)量取25.00mL烧碱溶液于锥形瓶中并加几滴甲基橙指示剂;
C.在天平上准确称取烧碱样品Wg,在烧杯中加蒸馏水溶解;
D.将物质的量浓度为Mmol/L的标准H2SO4溶液装入酸式滴定管,调整液面,记下开始刻度数为V1mL;
E.在锥形瓶下垫一张白纸,滴定到终点,记录终点刻度为V2mL.
请完成下列问题:
(1)操作步骤的正确顺序是(填写字母)C→A→B、D→E
(2)滴定至终点时,锥形瓶内溶液的pH约为4,终点时溶液颜色变化是溶液由黄色变为橙色,且半分钟内不恢复为原来的颜色
(3)若酸式滴定管没有用标准H2SO4溶液润洗,会对测定结果有何影响偏高.(填“偏高”、“偏低”或“无影响”,其他操作均正确)
(4)该烧碱样品的纯度计算式是$\frac{80M({V}_{1}-{V}_{2})}{W}$%.
分析 实验时应先称量一定质量的固体,溶解后配制成溶液,量取待测液与锥形瓶中,然后用标准液进行滴定,结合滴定操作的注意事项进行解答:
(1)实验时应先称量一定质量的固体,溶解后配制成溶液,量取待测液与锥形瓶中,然后用标准液进行滴定;
(2)指示剂为甲基橙,变色范围为3.1-4.4;指示剂为甲基橙,在碱性溶液中为黄色,滴定终点变橙色;
(3)因标准液浓度变小,用量变大;
(4)根据反应消耗的硫酸,求出氢氧化钠,进一步求出样品的纯度.
解答 解:(1)实验时应先称量一定质量的固体,溶解后配制成溶液,量取待测液与锥形瓶中,然后用标准液进行滴定,
故答案为:C;A;B;D;E;
(2)指示剂为甲基橙,变色范围为3.1-4.4,终点时pH约为4,溶液由黄色变为橙色,且半分钟内不恢复为原来的颜色,
故答案为:4;溶液由黄色变为橙色,且半分钟内不恢复为原来的颜色;
(3)若酸式滴定管没有用标准H2SO4溶液润洗,相当于标准液被稀释,导致标准液浓度变小,用量变大,使测定结果偏高,
故答案为:偏高;
(4)滴到消耗的硫酸为:n(硫酸)=cV=(V2-V1)×10-3L×M mol/L,根据反应方程可知,n(NaOH)=2n(硫酸)=2M(V2-V1)×10-3mol,
所以原来样品中氢氧化钠的物质的量为:2M(V2-V1)×10-3mol×$\frac{250}{25}$=2M(V2-V1)×10-2mol,
则样品中氢氧化钠的质量为m(NaOH)=n(NaOH)×M(NaOH)=2M(V2-V1)×10-2 mol×40 g/mol=80M(V2-V1)×10-2 g,则该烧碱样品的纯度为:$\frac{80M({V}_{2}-{V}_{1})×1{0}^{-2}g}{Wg}$×100%=$\frac{80M({V}_{1}-{V}_{2})}{W}$%,故答案为:$\frac{80M({V}_{1}-{V}_{2})}{W}$%.
点评 本题综合考查酸碱中和滴定,侧重于化学实验基本操作以及物质的含量的测定等问题,题目难度中等,建议在学习中把握相关基本实验方法,学习中注意积累.

| A. | cB=$\frac{ν_B}{ν_A}$•$\frac{{{c_A}{V_A}}}{V_B}$ | B. | cB=$\frac{ν_B}{ν_A}$•$\frac{{{c_A}{V_B}}}{V_A}$ | ||
| C. | cB=$\frac{{{c_A}{V_A}}}{V_B}$ | D. | cB=$\frac{ν_A}{ν_B}$•$\frac{{{c_A}{V_A}}}{V_B}$ |
已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+.
②某温度下一些金属氢氧化物的Ksp及开始沉淀和完全沉淀时的理论pH如表所示:
| M(OH)n | Ksp | pH | |
| 开始沉淀 | 沉淀完全 | ||
| Al(OH)3 | 2.0×10-32 | 4.1 | - |
| Fe(OH)3 | 3.5×10-38 | 2.2 | 3.5 |
| Fe(OH)2 | 1.0×10-15 | 7.5 | 9.5 |
| Ni(OH)2 | 6.5×10-18 | 6.4 | 8.4 |
(1)该电池的正极反应式为NiO2+2H2O+2e-=Ni(OH)2+2OH-;
(2)维持电流强度为1.0A,消耗0.02gFe,理论电池工作1.72min.(写出计算式,已知F=96500C/mol.)
(3)对该电池电极材料进行回收方案设计:
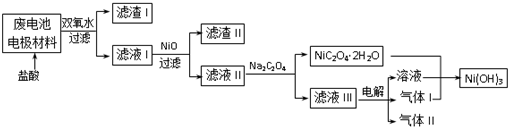
①方案中加入适量双氧水的目的是将溶液中的Fe2+氧化为Fe3+;在滤液I中慢慢加入NiO固体,则依次析出沉淀Fe(OH)3和沉淀Al(OH)3(填化学式).设计将析出的沉淀混合物中的两种物质分离开来的实验方案:将混合物加入氢氧化钠溶液充分溶解、过滤、洗涤得到滤渣为氢氧化铁,将滤液中通入过量二氧化碳气体过滤洗涤得到沉淀氢氧化铝.
②滤液Ⅲ中溶质的主要成分是NaCl(填化学式);气体I为Cl2,判断依据是电解氯化钠溶液,阳极上氯离子失电子生成氯气,Ni(OH)2-Ni(OH)3,镍元素化合价升高需要加入气体为氧化剂所以气体Ⅰ为Cl2.
| A. | 1 mol Cl2与过量的镁反应,转移 2NA个电子 | |
| B. | 常温常压下,16 g CH4含有 10NA个电子 | |
| C. | 1 mol•L -1 Na2SO4溶液中含有 NA个SO42- | |
| D. | 常温常压下,22.4 L CO2含有N A个CO2分子 |
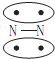 ,CO的结构可以表示为
,CO的结构可以表示为 ,其中椭圆框表示π键,下列说法中不正确的是 ( )
,其中椭圆框表示π键,下列说法中不正确的是 ( )| A. | N2分子与CO分子中都含有叁键 | |
| B. | CO分子中有一个π键是配位键 | |
| C. | N2、CO分别由非极性键和极性键结合,因此二者不是等电子体 | |
| D. | N2与CO的化学性质相同 |
| A. | 硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液:Fe2++2H++H2O2═Fe3++2H2O | |
| B. | 已知同温度下的溶解度:Zn(OH)2>ZnS,Na2S溶液与ZnCl2溶液混合:Zn2++S2-+2H2O═Zn(OH)2↓+H2S↑ | |
| C. | 0.01 mol•L-1NH4Al(SO4)2溶液与0.02 mol•L-1 Ba(OH)2溶液等体积混合:Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O | |
| D. | 向KI-淀粉溶液中加入稀硫酸,在空气中放置一段时间后,溶液呈蓝色:4H++4I-+O2═2I2+2H2O |
 .W、X、Y的离子半径由大到小的顺序为S2->O2->Al3+(用离子符号回答)
.W、X、Y的离子半径由大到小的顺序为S2->O2->Al3+(用离子符号回答)