题目内容
5.下列说法不正确的是( )| A. | 铁在纯氧中燃烧或高温下和水蒸气反应均能得到Fe3O4 | |
| B. | NaCl溶液能导电是因为溶液中有自由移动的Na+和Cl- | |
| C. | 进行焰色反应,连续做两个样品时,应将铂丝用硫酸洗净并灼烧到无特殊焰色 | |
| D. | 浓硫酸不慎沾在皮肤上,应立即用干布拭去,然后用水冲洗,最后再涂上3%-5%的小苏打溶液 |
分析 A、铁在氧气中燃烧生成四氧化三铁,和水蒸气反应生成四氧化三铁和氢气;
B、含有自由移动离子或自由移动电子的物质能导电;
C、进行焰色反应,应将铂丝用盐酸洗净,盐酸具有挥发性;
D、因浓硫酸能与水反应会发热,如果用水清洗会增大烧伤面积,则先用抹布擦拭,再用大量的水冲洗,冲洗后皮肤上呈弱酸性,一般用弱碱性溶液来处理.
解答 解:A、铁在氧气中燃烧生成四氧化三铁,和水蒸气反应生成四氧化三铁和氢气,铁在纯氧中燃烧或高温下和水蒸气反应均能得到Fe3O4,故A正确;
B、氯化钠溶液中含有自由移动的阴阳离子,在电流作用下能定向移动,所以能导电,故B正确;
C、进行焰色反应,应将铂丝用盐酸洗净,盐酸具有挥发性,不能用硫酸来洗铂丝,故C错误;
D、因浓硫酸能与水反应会发热,如果用水清洗会增大烧伤面积,则先用抹布擦拭,再用大量的水冲洗,冲洗后皮肤上呈弱酸性,涂上3%~5%的小苏打溶液,故D正确;
故选C.
点评 本题考查学生元素化合物的有关知识,注意知识的归纳和梳理是关键,难度中等.

练习册系列答案
相关题目
11.已知 X、Y、Z、M、R五种元素中,原子序数X<Y<Z<M<R,其结构或性质信息如下表.请根据信息回答有关问题:
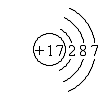
(1)元素M的原子核外共有17种不同运动状态的电子,有5种不同能级的电子.
(2)X、Y、Z三种元素的第一电离能较高的是N(写元素符号),原因是N原子的2p能级电子为半充满,为较稳定的结构.
(3)R的一种配合物的化学式为RCl3•6H2O.已知0.01molRCl3•6H2O在水溶液中用过量硝酸银溶液处理,产生0.02mol AgCl沉淀.此配合物最可能是B.
A.[R(H2O)6]Cl3 B.[R(H2O)5Cl]Cl2•H2O C.[R(H2O)4Cl2]Cl•2H2O D.[R(H2O)3Cl3]•3H2O.
| 元素 | 结构或性质信息 |
| X | 原子的L层上s电子数等于p电子数. |
| Y | 原子核外的L层有3个未成对电子. |
| Z | 在元素周期表的各元素中电负性仅小于氟. |
| M | 单质常温、常压下是气体,原子的M层上有1个未成对的p电子. |
| R | 第四周期过渡元素,其价电子层各能级处于半充满状态 |
(2)X、Y、Z三种元素的第一电离能较高的是N(写元素符号),原因是N原子的2p能级电子为半充满,为较稳定的结构.
(3)R的一种配合物的化学式为RCl3•6H2O.已知0.01molRCl3•6H2O在水溶液中用过量硝酸银溶液处理,产生0.02mol AgCl沉淀.此配合物最可能是B.
A.[R(H2O)6]Cl3 B.[R(H2O)5Cl]Cl2•H2O C.[R(H2O)4Cl2]Cl•2H2O D.[R(H2O)3Cl3]•3H2O.
12.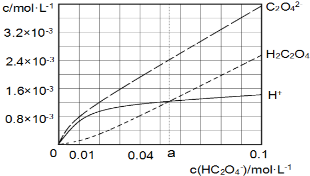 25℃时,往水中不断加入NaHC2O4固体,部分微粒浓度随c(HC2O4)的变化趋势如下图所示.下列说法正确的是( )
25℃时,往水中不断加入NaHC2O4固体,部分微粒浓度随c(HC2O4)的变化趋势如下图所示.下列说法正确的是( )
 25℃时,往水中不断加入NaHC2O4固体,部分微粒浓度随c(HC2O4)的变化趋势如下图所示.下列说法正确的是( )
25℃时,往水中不断加入NaHC2O4固体,部分微粒浓度随c(HC2O4)的变化趋势如下图所示.下列说法正确的是( )| A. | 当c(HC2O4ˉ)=0.1mol•Lˉ1时,c(H+)>c(C2O42-)-c(H2C2O4) | |
| B. | 当c(HC2O4ˉ)>amol•Lˉ1时,c(H+)<c(H2C2O4),HC2O4ˉ的水解程度大于电离程度 | |
| C. | HC2O4ˉ?C2O42-+H+,Ka(HC2O4ˉ)=a | |
| D. | 将0.08mol•Lˉ1H2C2O4溶液与等浓度NaOH溶液等体积混合后(忽略体积变化),c(Na+)>c(HC2O4ˉ)>c(C2O42-)>c(H2C2O4)>c(H+)>c(OHˉ) |
20.生物质能是一种洁净、可再生能源.生物质气(主要成分为 CO、CO2、H2 等)与H2混合,催化合成甲醇和二甲醚(CH3OCH3)及许多烃类物质等,是生物质能利用的方法之一.
(1)已知碳的气化反应在不同温度下平衡常数的对数值(lgK)如下表:
反应:CO(g)+H2O(g)?CO2(g)+H2(g),该反应的△H<0(选填:“>”、“<”、“=”);在900K时,该反应平衡常数的对数值(lgK)=0.36.
(2)业上合成甲醇的反应为:CO+2H2?CH3OH.已知:H2(g)、CO(g)、CH3OH(l)的燃烧热△H分别为-285.8kJ/mol、-283.0kJ/mol和-726.5kJ/mol.则:CH3OH(l)不完全燃烧生成CO和液态H2O的热化学反应方程式为CH3OH(l)+O2(g)=CO(g)+2H2O(l);△H=-443.5kJ/mol.
(3)在一定温度、压强和催化条件下,工业上用H2CO和CO合成CH3OCH3:
3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)△H=-246.4KJ•mol-1
①在一定条件下的密闭容器中,该反应达到平衡,只改变一个条件能同时提高反应速率和CO的转化率的是cd(填字母序号).
a.降低温度 b.加入催化剂 c.缩小容器体积 d.增加H2的浓度 e.增加CO的浓度
②在一体积可变的密闭容器中充入3molH2、3molCO、1molCH3OCH3、1molCO2,在一定温度和压强下发生上述反应,经一定时间达到平衡,测得平衡时混合气体的密度是同温同压下起始的1.6倍.反应开始时正、逆反应速率的大小:v正>v逆(填“>”“<”或“=”),平衡时CO的物质的量分数为15%.
(4)一定条件下可用甲醇与CO反应生成醋酸消除CO污染,常温下,将amol•L-1的醋酸与bmol•L-1的Ba(OH)2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(CH3COO-),则该混合溶液中醋酸的电离常数Ka=$\frac{2b}{a-2b}$×10-7 mol•L-1(用含a和b的代数式表示,体积变化忽略不计).
(1)已知碳的气化反应在不同温度下平衡常数的对数值(lgK)如下表:
| 气化反应式 | 1gK | ||
| 700K | 900K | 1200K | |
| C(s)+H2O(g)=CO(g)+H2(g) | -2.64 | -0.39 | 1.58 |
| C(s)+2H2O(g)=CO2(g)+2H2(g) | -1.67 | -0.03 | 1.44 |
(2)业上合成甲醇的反应为:CO+2H2?CH3OH.已知:H2(g)、CO(g)、CH3OH(l)的燃烧热△H分别为-285.8kJ/mol、-283.0kJ/mol和-726.5kJ/mol.则:CH3OH(l)不完全燃烧生成CO和液态H2O的热化学反应方程式为CH3OH(l)+O2(g)=CO(g)+2H2O(l);△H=-443.5kJ/mol.
(3)在一定温度、压强和催化条件下,工业上用H2CO和CO合成CH3OCH3:
3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)△H=-246.4KJ•mol-1
①在一定条件下的密闭容器中,该反应达到平衡,只改变一个条件能同时提高反应速率和CO的转化率的是cd(填字母序号).
a.降低温度 b.加入催化剂 c.缩小容器体积 d.增加H2的浓度 e.增加CO的浓度
②在一体积可变的密闭容器中充入3molH2、3molCO、1molCH3OCH3、1molCO2,在一定温度和压强下发生上述反应,经一定时间达到平衡,测得平衡时混合气体的密度是同温同压下起始的1.6倍.反应开始时正、逆反应速率的大小:v正>v逆(填“>”“<”或“=”),平衡时CO的物质的量分数为15%.
(4)一定条件下可用甲醇与CO反应生成醋酸消除CO污染,常温下,将amol•L-1的醋酸与bmol•L-1的Ba(OH)2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(CH3COO-),则该混合溶液中醋酸的电离常数Ka=$\frac{2b}{a-2b}$×10-7 mol•L-1(用含a和b的代数式表示,体积变化忽略不计).
17.在通常条件下,下列各组物质的性质排列正确的是( )
| A. | 熔点:Na>MgO>SiO2 | B. | 水溶性:SO2>H2S>HCl | ||
| C. | 热稳定性:HF>H2O>NH3 | D. | 沸点:HF>HCl>HBr |
14.下面的排序不正确的是( )
| A. | 晶体熔点由低到高:CF4<CCl4<CBr4<CI4 | |
| B. | 熔点由高到低:Na>Mg>Al | |
| C. | 硬度由大到小:金刚石>碳化硅>晶体硅 | |
| D. | 四种气态氢化物按稳定性:SiH4<CH4<H2O<HF |
 有如下化学反应:2A(g)+B(g)?2C(g),△H<0.
有如下化学反应:2A(g)+B(g)?2C(g),△H<0.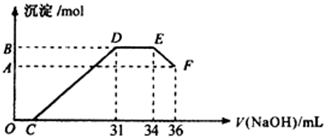
 .
.