题目内容
氢气是未来最理想的能源,科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术 2H2
2H2↑+O2↑.制得的氢气可用于燃料电池.试回答下列问题:
(1)分解海水时,实现了从 能转化为 能,二氧化钛作 .生成的氢气用于燃料电池时,实现 能转化为 能.水分解时,断裂 键,分解海水的反应属于 反应(填“放热”或“吸热”).
(2)某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,两极上分别通入氢气和氧气,发生的电池反应为2H2+O2=2H2O.则通入氢气的一极是电池的 极,电流从该极 (填“流入”或“流出”).
| ||
| TiO2 |
(1)分解海水时,实现了从
(2)某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,两极上分别通入氢气和氧气,发生的电池反应为2H2+O2=2H2O.则通入氢气的一极是电池的
考点:原电池和电解池的工作原理,吸热反应和放热反应
专题:
分析:(1)太阳光分解海水时,太阳能转化为化学能,二氧化钛做催化剂;燃料电池是将化学能转变为电能的装置;水的分解为吸热反应,在催化剂的条件下生成氢气和氧气,断裂的化学键为H-O;
(2)氢氧燃料电池中,氢气在负极失电子发生氧化反应,氧气在正极得电子发生还原反应,电流从正极流向负极.
(2)氢氧燃料电池中,氢气在负极失电子发生氧化反应,氧气在正极得电子发生还原反应,电流从正极流向负极.
解答:
解:(1)太阳光分解海水时,太阳能转化为化学能,水难以分解,在二氧化钛(TiO2)表面作用使海水分解得到氢气,并用激光提供能量,则说明二氧化钛起到催化剂的作用,燃料电池是将化学能转变为电能的装置;氢气和氧气的燃烧为放热反应,则水分解时,水分子中的H-O断裂生成氧原子和氢原子,该反应吸热反应,
故答案为:太阳;化学;催化剂;化学;电;H-O;吸热;
(2)氢氧燃料电池中,氢气在负极失电子发生氧化反应,氧气在正极得电子发生还原反应,电流从正极流向负极,故答案为:负;流入.
故答案为:太阳;化学;催化剂;化学;电;H-O;吸热;
(2)氢氧燃料电池中,氢气在负极失电子发生氧化反应,氧气在正极得电子发生还原反应,电流从正极流向负极,故答案为:负;流入.
点评:本题考查了能量的转化形式及放热反应等知识点,题目难度不大,注意掌握常见的能量转化形式,明确化学反应与能量变化的关系.

练习册系列答案
相关题目
下列离子方程式正确的是( )
| A、铁粉和氯化铁溶液反应 Fe+Fe3+═Fe2+ |
| B、铁和稀盐酸反应 Fe+2H+═Fe2++H2↑ |
| C、氯气通入水中:Cl2+H2O=2H++Cl-+ClO- |
| D、铝和氢氧化钠溶液反应 2Al+2OH-=2AlO2-+3H2↑ |
短周期主族元素X、Y、Z、W原子序数依次增大,已知Y是四种元素中金属性最强的元素,Y、Z、W同周期,且三种元素原子的最外层电子数之和为11,X2-和Y+具有相同的电子层结构,下列叙述正确的是( )
| A、离子半径:X2->Y+ |
| B、原子的最外层电子数:X>Y>Z>W |
| C、单质沸点:X>Y>Z>W |
| D、X与Y形成的化合物中只2含有离子键 |
下列有机物命名正确的是( )
| A、2,3,3-三甲基丁烷 |
| B、2-乙基戊烷 |
| C、3-乙基-1-戊烯 |
| D、2,2-二甲基-1-丁烯 |
用石墨作电极电解0.1mol?L-1的CuSO4溶液,当有0.4mol电子通过电路时,发现阴极增重6.4g,则要使电解后的溶液恢复到原始状态,则应向电解后的溶液中加入( )
| A、0.1molCu(OH)2 |
| B、0.1molCuO |
| C、0.2molCuO |
| D、0.1molCuO和0.2molH2O |
下列有关浓硫酸的说法正确的是( )
| A、若大量浓硫酸洒在皮肤上应立即用纱布拭去,再用大量水冲洗 |
| B、稀释时要将水沿器壁慢慢倒入浓硫酸中,并用玻璃棒不断搅拌 |
| C、欲除去NH3中的H2O,可让混合气体通过盛有浓硫酸的洗气瓶 |
| D、浓硫酸不分解,不挥发,所以能敞口放置在空气中,质量不会发生变化 |
浓硫酸在加热条件下能溶解金属银,反应的化学方程式为2Ag+2H2SO4 (浓)
Ag2SO4+SO2↑+2H2O,下列反应中浓硫酸的作用与该反应相同的是( )
| △ |
A、Cu+2H2SO4 (浓)
| ||
B、C+2H2SO4 (浓)
| ||
| C、2FeO+4H2SO4→Fe2(SO4)3+SO2↑+4H20 | ||
D、C2H5OH+2H2SO4 (浓)
|
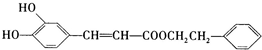 是一种天然抗癌药物,在一定条件下能发生如下转化:
是一种天然抗癌药物,在一定条件下能发生如下转化: