题目内容
4.设NA为阿伏加德罗常数的值,下列叙述正确的是( )| A. | 标准状况下,33.6 L氟化氢中含有氟原子的数目为1.5NA | |
| B. | 常温常压下,Na2O2与足量H2O反应,共生成0.2 mol O2,转移电子数目为0.4NA | |
| C. | 1 L 1 mol?•L-1 FeCl3完全水解生成NA个胶体粒子 | |
| D. | 含2 mol H2SO4的浓硫酸与足量的铜片在加热条件下完全反应,可产生NA个SO2气体分子 |
分析 A、标况下HF为液态;
B、过氧化钠与水的反应中,氧元素的价态由-1价变为0价;
C、一个氢氧化铁胶粒是多个氢氧化铁的聚集体;
D、铜只能与浓硫酸反应,与稀硫酸不反应.
解答 解:A、标况下HF为液态,故不能根据气体摩尔体积来计算其物质的量和含有的F原子个数,故A错误;
B、过氧化钠与水的反应中,氧元素的价态由-1价变为0价,故当生成0.2mol氧气时,转移的电子数为0.4NA个,故B正确;
C、一个氢氧化铁胶粒是多个氢氧化铁的聚集体,故生成的胶粒个数小于NA个,故C错误;
D、铜只能与浓硫酸反应,与稀硫酸不反应,故浓硫酸不能反应完全,则生成的气体分子小于NA个,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
15.同温同压下,相同质量的下列气体中,体积最大的是( )
| A. | N2 | B. | SO2 | C. | Cl2 | D. | CO2 |
19.分子式为C5H11Cl并含两个甲基的有机物的同分异构体共几种(不含立体异构)( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
9.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 常温常压下的33.6 L氯气与27 g铝充分反应,转移电子数为3NA | |
| B. | 常温下,46 g分子式为C2H6O的物质中一定含有极性键为7NA,非极性键为NA | |
| C. | 125 mL 16 mol/L浓硫酸与足量的铜反应,生成SO2的分子数小于NA | |
| D. | 标准状况下,体积为22.4 L NO2、N2O4的混合气体,升温至常温,则混合气体分子数为NA |
13.下列有关乙烯的说法,其中错误的是( )
| A. | 乙烯分子的双键中有一键较易断裂 | |
| B. | 烯分子里所有原子都在同一个平面上,且碳氢键之间的键角约为120° | |
| C. | 乙烯的化学性质比乙烷活泼 | |
| D. | 乙烯和环丙烷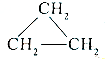 的分子组成符合通式CnH2n,因此它们属于同系物 的分子组成符合通式CnH2n,因此它们属于同系物 |

 .
.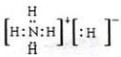 .
.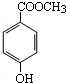 .
. ,其中包含的反应类型有取代反应或水解反应、中和反应.
,其中包含的反应类型有取代反应或水解反应、中和反应.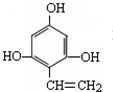 、
、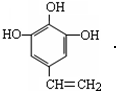 .
.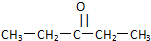
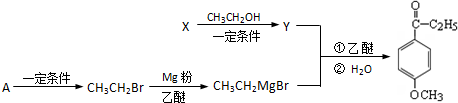
 .
.