题目内容
2gAO
中电子数比质子数多3.01×1022个,则A的相对原子质量为 .
2- 3 |
考点:物质的量的相关计算
专题:计算题
分析:从离子的化学式可以看出,每个AO32-带2个单位的负电荷,表明电子总数比质子总数多2.现在电子比质子多3.01×1022,也就是有3.01×1022÷2=1.505×1022个AO32-离子,这些AO32-离子的物质的量为1.505×1022÷(6.02×1023/mol)=0.025mol,由此分析求元素A的相对原子质量.
解答:
解:从离子的化学式可以看出,每个AO32-带2个单位的负电荷,表明电子总数比质子总数多2.现在电子比质子多3.01×1022,也就是有3.01×1022÷2=1.505×1022个AO32-离子,这些AO32-离子的物质的量为1.505×1022÷(6.02×1023/mol)=0.025mol,其质量题中已给出,为2g,则其摩尔质量为2g÷0.025mol=80g/mol,元素A的相对原子质量为:80-16×3=32,故答案为:32.
点评:本题考查根据微粒的组成结合物质的量的变化,求相对原子质量,学生只要抓住电子数比质子数多多少列出关系式,就可以迅速解题了,比较容易.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
下列叙述正确的是( )
| A、固体氯化钠不导电,所以氯化钠不是电解质 |
| B、虽然NaHSO4溶于水能电离出H+,但它不是酸 |
| C、“纳米材料”是粒子直径1~100 nm的材料,它属于胶体 |
| D、在一个氧化还原反应中,有一种元素被氧化肯定有另一种元素被还原 |
下列离子方程式书写不正确的是( )
A、以石墨作电极电解NaCl溶液:2Cl-+2H2O
| ||||
B、用Pt作电极电解CuSO4溶液:2Cu2++2H2O
| ||||
| C、AlCl3溶液中加入过量稀氨水:Al3++4NH3?H2O=AlO2-+4NH4++2H2O | ||||
| D、NaAlO2溶液中通入过量的CO2:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- |
在反应2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O中,有0.8mol HCl参与反应,则电子转移的个数为( )
| A、3.01×1023 |
| B、4.816×1023 |
| C、6.02×1023 |
| D、1.204×1024 |
当光束通过下列分散系时,能观察到丁达尔效应的是( )
| A、盐酸 | B、氢氧化铁胶体 |
| C、氯化钠溶液 | D、硫酸铜溶液 |
设NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A、常温常压下,16 g CH4中含有的原子总数为5NA |
| B、标准状况下,11.2 LCH3OH中含有的共价键数目为2.5NA |
| C、常温常压下,2.24 L CO和CO2混合气体中含有的碳原子数目为0.1NA |
| D、标准状况下,0.1 mol Cl2被氢氧化钠溶液完全吸收,转移的电子数目为0.2NA |
奶粉行业的“911事件”将三聚氰胺引入公众视野,工业上可用尿素为原料,在一定条件下合成三聚氰胺:
6CO(NH2)2→6NH3+3CO2+C3H6N6,对C3H6N6说法正确的是( )
6CO(NH2)2→6NH3+3CO2+C3H6N6,对C3H6N6说法正确的是( )
| A、摩尔质量为126 |
| B、式量为126g?mol-1 |
| C、每个C3H6N6分子含3个N2分子 |
| D、0.1 mol-1C3H6N6含碳原子数为1.806×1023 |
已知CuS、PbS、HgS的溶度积分别为l.3×l0-36、9.0×10-29、6.4×10-23.下列推断不正确的是( )
| A、硫化钠是处理废水中含上述金属离子的沉淀剂 |
| B、在硫化铅悬浊液中滴几滴硝酸铜溶液,会生成硫化铜 |
| C、在含Hg2+、Cu2+、Pb2+的溶液中滴加硫化钠溶液,当c(S2-)=0.001 mol?L-1时三种金属离子都完全沉淀 |
| D、向含Pb2+、Cu2+、Hg2+的浓度均为0.010 mol?L-1的溶液中通人硫化氢气体,产生沉淀的顺序依次为PbS、CuS、HgS |
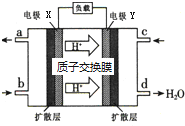 绿色电源“二甲醚-氧气燃料电池”的工作原理如图,
绿色电源“二甲醚-氧气燃料电池”的工作原理如图,