题目内容
镍氢电池是近年开发出来的可充电电池,它可以取代会产生镉污染的镉镍电池.氢镍电池的总反应式是:
H2+NiO(OH)=Ni(OH)2据此反应式判断,下列叙述中正确的是( )
| 1 |
| 2 |
| A、电池放电时,电池负极周围的溶液pH不断增大 |
| B、电池放电时,镍元素被氧化 |
| C、电池放电时,镍元素被还原 |
| D、电池放电时,H2是负极 |
考点:化学电源新型电池
专题:电化学专题
分析:氢镍电池的总反应式是:
H2+NiO(OH)=Ni(OH)2,放电时,负极反应为:H2-2e-+2OH-=2H2O,正极反应为:NiO(OH)+H2O+e-=OH-+Ni(OH)2,充电时的电极反应为放电时的逆反应.
| 1 |
| 2 |
解答:
解:A、电池放电时,负极反应式为:H2-2e-+2OH-=2H2O,所以电池周围溶液的氢氧根离子减少,溶液的PH值减小,故A错误.
B.电池放电时,正极反应为:NiO(OH)+H2O+e-=OH-+Ni(OH)2,镍元素被还原,故B错误;
C.电池放电时,正极反应为:NiO(OH)+H2O+e-=OH-+Ni(OH)2,镍元素被还原,故C正确;
D.电池放电时,负极反应为H2-2e-+2OH-=2H2O,H2是负极,故D正确;
故选CD.
B.电池放电时,正极反应为:NiO(OH)+H2O+e-=OH-+Ni(OH)2,镍元素被还原,故B错误;
C.电池放电时,正极反应为:NiO(OH)+H2O+e-=OH-+Ni(OH)2,镍元素被还原,故C正确;
D.电池放电时,负极反应为H2-2e-+2OH-=2H2O,H2是负极,故D正确;
故选CD.
点评:本题考查化学电源新型电池,题目难度不大,注意电极反应式的书写,根据电极反应判断溶液离子浓度的变化.

练习册系列答案
相关题目
在无色透明的溶液中可以大量共存的离子组是( )
| A、H+、K+、HCO3-、NO3- |
| B、OH-、Cl-、Na+、NH4+ |
| C、Cu2+、NO3-、OH-、Cl- |
| D、Mg2+、H+、Cl-、NO3- |
当光束通过下列分散系时,能观察到丁达尔效应的是( )
| A、盐酸 | B、氢氧化铁胶体 |
| C、氯化钠溶液 | D、硫酸铜溶液 |
奶粉行业的“911事件”将三聚氰胺引入公众视野,工业上可用尿素为原料,在一定条件下合成三聚氰胺:
6CO(NH2)2→6NH3+3CO2+C3H6N6,对C3H6N6说法正确的是( )
6CO(NH2)2→6NH3+3CO2+C3H6N6,对C3H6N6说法正确的是( )
| A、摩尔质量为126 |
| B、式量为126g?mol-1 |
| C、每个C3H6N6分子含3个N2分子 |
| D、0.1 mol-1C3H6N6含碳原子数为1.806×1023 |
下列过程没有发生化学反应的是( )
| A、用活性炭去除冰箱中的异味 |
| B、用热碱水清除炊具上残留的油渍 |
| C、用浸泡过高锰酸钾溶液的砖头储存水果 |
| D、用含硅胶、铁粉的透气小袋与食品一起密封包装 |
取一定量FeO和Fe2O3的混合物,在H2流中加热充分反应.冷却,称得剩余固体比原混合物质量减少1.200g,若将同量的该混合物与盐酸反应完全,至少需1mol/L盐酸的体积为( )
| A、37.5mL |
| B、75mL |
| C、150mL |
| D、300mL |
某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )


| A、加入Na2SO4可以使溶液由a点变到c点 |
| B、通过蒸发可以使溶液由d点变到c点 |
| C、b点无BaSO4沉淀生成 |
| D、a点对应的Ksp大于c点对应的Ksp |
下列说法中,不正确的是( )
| A、分液操作时,分液漏斗下端管口尖端处紧靠烧杯内壁 |
| B、利用丁达尔效应可鉴别溶液和胶体 |
| C、二氧化硅能用于制造光导纤维 |
| D、用pH试纸测定某溶液的pH时,需预先用蒸馏水湿润pH试纸 |
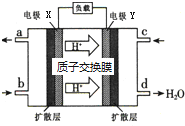 绿色电源“二甲醚-氧气燃料电池”的工作原理如图,
绿色电源“二甲醚-氧气燃料电池”的工作原理如图,