题目内容
13.设NA表示阿伏加德罗常数的数值,下列说法不正确的是( )| A. | 14g由N2和13C2H2组成的混合物所含的电子数为7NA | |
| B. | 1mol氨基(-NH2)中含有电子数目为10NA | |
| C. | 一定条件下,1molN2和3molH2充分反应,转移电子数目为2NA | |
| D. | 常温下,1LPH=3的Al2(SO4)3溶液中,水电离出的H+数目为10-3NA |
分析 A.N2和13C2H2分子中都含有14个电子,二者摩尔质量都是28g/mol;
B.-NH2中含有9个电子,1mol氨基中含有9mol电子;
C.氮气与氢气的反应为可逆反应,无法计算该反应中转移电子的物质的量及数目;
D.铝离子水解促进了水的电离,硫酸铝溶液中的氢离子来自水的电离.
解答 解:A.14g由N2和13C2H2组成的混合物含有分子的物质的量为:$\frac{14g}{28g/mol}$=0.5mol,0.5molN2和13C2H2组成的混合物中含有电子的物质的量为:0.5mol×14=7mol,则该混合物中所含的电子数为7NA,故A正确;
B.1mol氨基(-NH2)中含有9mol电子,含有电子数目为9NA,故B错误;
C.一定条件下1molN2和3molH2充分反应,由于该反应为可逆反应,题中缺少生成氨气的量,则无法计算转移电子数目,故C错误;
D.常温下1L pH=3的Al2(SO4)3溶液中氢离子浓度为10-3mol/L,由于铝离子水解促进了水的电离,该溶液中的氢离子来自水的电离,则水电离出的氢离子的物质的量为10-3mol,水电离的H+数目为10-3NA,故D正确;
故选BC.
点评 本题考查阿伏加德罗常数的计算与判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系;试题有利于,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
4.对于反应:Cu+4HNO3→Cu(NO2)2+2NO2↑+2H2O,下列叙述中正确的是( )
①这是置换反应②反应中被还原的是HNO3③所用硝酸是稀溶液④所用硝酸是浓溶液.
①这是置换反应②反应中被还原的是HNO3③所用硝酸是稀溶液④所用硝酸是浓溶液.
| A. | ①④ | B. | ①③ | C. | ②③ | D. | ②④ |
1.下列说法不正确的是( )
| A. | 单晶硅是石英的主要成分 | |
| B. | 钠钾合金可用与快中子反应堆的热交换剂 | |
| C. | 小苏打可用于焙制糕点 | |
| D. | 水玻璃暴露在空气中会发生变质 |
18.将SO2通入BaCl2溶液至饱和,未见有沉淀生成,继续通入另一种气体后仍然无沉淀产生,此气体是( )
| A. | CO2 | B. | NH3 | C. | NO2 | D. | HCl |
5.某可逆反应达到化学平衡,当条件改变后平衡向正反应方向移动.则下列说法中正确的是( )
| A. | 反应物的浓度一定降低 | B. | 正反应速率一定大于逆应速率 | ||
| C. | 使用了合适的催化剂 | D. | 生成物的百分含量增大 |
3.如图所示的是验证SO2性质的微型实验,a、b、c、d是浸有相关溶液的棉球.将硫酸滴入装有亚硫酸钠固体的培养皿.
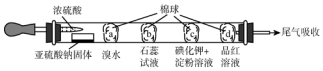
关于此实验的“现象”、“解释或结论”以及对应关系均正确的是( )

关于此实验的“现象”、“解释或结论”以及对应关系均正确的是( )
| 选项 | 现象 | 解释和结论 |
| A | a处橙色褪去 | 还原性:Br->SO2 |
| B | b处先变为红色后褪色 | SO2能与H2O反应,且有漂白性 |
| C | c处变为蓝色 | SO2具有一定的氧化性 |
| D | d处红色褪去 | SO2具有漂泊性 |
| A. | A | B. | B | C. | C | D. | D |