题目内容
8.氨基酸在溶液中按两种方式电离以下判断正确的是( )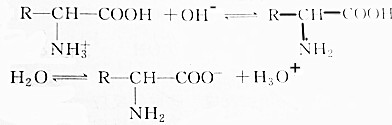
| A. | 增大溶液的pH,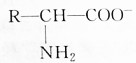 浓度减小 浓度减小 | |
| B. | 降低溶液的pH,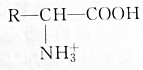 浓度减小 浓度减小 | |
| C. | 如溶液的pH适当,两种氨基酸离子的浓度可能相同 | |
| D. | pH改变,对电离方式无影响 |
分析 A.增大溶液的pH,c(H3O+)减小,平衡正向移动;
B.降低溶液的pH,c(H3O+)增大,平衡逆向移动;
C.根据电荷守恒,当溶液呈中性时,两种氨基酸离子的浓度可能相同;
D.pH改变影响电离平衡的移动方向.
解答 解:A.增大溶液的pH,c(H3O+)减小,平衡正向移动,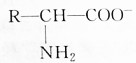 浓度增大,故A错误;
浓度增大,故A错误;
B.降低溶液的pH,c(H3O+)增大,平衡逆向移动,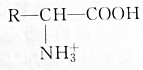 的浓度增大,故B错误;
的浓度增大,故B错误;
C.根据电荷守恒,当溶液呈中性时,两种氨基酸离子的浓度可能相同,故C正确;
D.pH改变影响电离平衡的移动方向,故D错误;
故选C.
点评 本题考查电离平衡的移动,难度难度中等,明确pH的变化对电离平衡的影响和电荷守恒思想的应用是解题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
18.反应N2+3H2=2NH3的能量变化如图所示,该反应的热化学方程式是( )

| A. | N2(g)+3H2(g)═2NH3(l)△H=2(a-b-c) kJ•mol-1 | |
| B. | N2(g)+3H2(g)═2NH3(g)△H=2(b-a) kJ•mol-1 | |
| C. | $\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)═NH3(l)△H=2(b+c-a) kJ•mol-1 | |
| D. | $\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)═NH3(g)△H=2(a+b) kJ•mol-1 |
19.能正确表示下列反应的离子方程式是( )
| A. | 硫酸铝溶液中加入过量氨水:Al3++4OH-═AlO2-+2H2O | |
| B. | 浓盐酸与铁屑反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 钠与CuSO4溶液反应:2Na+Cu2+═Cu↓+2Na+ | |
| D. | 在8.12天津大爆炸中消防员喷洒双氧水以防止氰化钠污染环境:CN-+H2O2+H2O═HCO3-+NH3↑ |
3.将NO2与氧气以一定比例通入足量水中,得到溶液,关于这份溶液,下列说法正确的是( )
| A. | 若NO2与O2的体积比是4:3,则此溶液除了硝酸不含其他杂质 | |
| B. | 将一定量的Cu投入溶液中,只产生1.12L(标况)的红棕色气体,则反应的铜有1.6g | |
| C. | 将溶液在强光下光照,产生气泡,溶液变浅黄,产生气泡,则气泡是NO2 | |
| D. | 向浅黄的硝酸中通入氧气,可以使其pH值降低,溶液质量不变 |
13.研究发现,镭能蜕变为${\;}_{86}^{222}$Rn,故将${\;}_{86}^{222}$Rn称为镭射气.钍能衰变为${\;}_{86}^{220}$Rn,故将 ${\;}_{86}^{220}$Rn称为钍射气;锕能衰变为${\;}_{86}^{219}$Rn,故将${\;}_{86}^{219}$Rn称为锕射气.${\;}_{86}^{222}$Rn、${\;}_{86}^{220}$Rn、${\;}_{86}^{219}$Rn( )
| A. | 属于同种元素 | B. | 属于同位素 | C. | 属于同种核素 | D. | 属于同种原子 |
20.下列变化中,只破坏了共价键的是( )
| A. | 干冰气化 | B. | 氯酸钾受热分解 | C. | 氯化钠溶于水 | D. | 晶体硅熔化 |
17.下列说法正确的是( )
| A. | 乙醇制乙醛、乙酸制乙酸乙酯均为取代反应 | |
| B. | 乙烯制聚乙烯、苯制硝基苯均发生加聚反应 | |
| C. | 蛋白质盐析、糖类水解均为化学变化 | |
| D. | 石油分馏、煤干馏均可得到烃 |
1.下列说法正确的是( )
| A. | 改变条件,反应物的转化率增大,平衡常数也一定增大 | |
| B. | 常温下,V1L pH=12的NaOH溶液与V2L pH=2的HA溶液混合,若混合液显中性,则V1≤V2 | |
| C. | 在0.1mol•L-1 NaHCO3溶液中,加入少量NaOH固体,Na+和CO32-的离子浓度均增大 | |
| D. | 原子晶体与分子晶体在溶于水和熔化时化学键均断裂 |
