题目内容
16.三氯化铬是化学合成中的常见物质,三氯化铬易升华,在高温下能被氧气氧化.制备三氯化铬的流程如图所示:
(1)重铬酸铵分解产生的三氧化二铬(Cr2O3难溶于水)需用蒸馏水洗涤,如何用简单方法判断其已洗涤干净?最后一次洗涤的流出液呈无色.
(2)已知CCl4沸点为76.8℃,为保证稳定的CCl4气流,适宜的加热方式是水浴加热(并用温度计指示温度).
(3)用图2装置制备CrCl3时,反应管中发生的主要反应为:Cr2O3+3CCl4═2CrCl3+3COCl2,则向三颈烧瓶中通入N2的作用:
①赶尽反应装置中的氧气;
②鼓气使反应物进入管式炉中进行反应.
(4)样品中三氯化铬质量分数的测定:称取样品0.3000g,加水溶解并定容于250mL容量瓶中.移取25.00mL于碘量瓶(一种带塞的锥形瓶)中,加热至沸后加入1g Na2O2,充分加热煮沸,适当稀释,然后加入过量2mol•L-1H2SO4至溶液呈强酸性,此时铬以Cr2O72-存在,再加入1.1g KI,加塞摇匀,充分反应后铬以Cr3+存在,于暗处静置5min后,加入1mL指示剂,用0.0250mol•L-1标准Na2S2O3溶液滴定至终点,平行测定三次,平均消耗标准Na2S2O3溶液21.00mL.(已知:2Na2S2O3+I2═Na2S4O6+2NaI)
①滴定实验可选用的指示剂名称为淀粉,判定终点的现象是最后一滴滴入时,蓝色恰好完全褪去,且半分钟内不恢复原色;若滴定时振荡不充分,刚看到局部变色就停止滴定,则会使样品中无水三氯化铬的质量分数的测量结果_偏低(填“偏高”“偏低”或“无影响”).
②加入Na2O2后要加热煮沸,其主要原因是除去其中溶解的氧气,防止氧气将I-氧化,产生偏高的误差.
③加入KI时发生反应的离子方程式为Cr2O72-+6I-+14H+═2Cr3++3I2+7H2O.
④样品中无水三氯化铬的质量分数为92.5%.(结果保留一位小数)
分析 根据流程图知,重铬酸铵分解产生的三氧化二铬(Cr2O3难溶于水)、氮气和水,然后洗涤、烘干得到Cr2O3,在加热条件下,在反应器中发生反应Cr2O3+3CCl4═2CrCl3+3COCl2,三氯化铬易升华,在高温下能被氧气氧化,为防止三氯化铬被氧化,通入氮气,且充入的氮气能使反应物进入管式炉中进行反应;最后得到无水三氯化铬;
(1)重铬酸铵分解不完全,还可能含有其它可溶性杂质;因为(NH4)2Cr2O7显桔红色,所以可以提供颜色来判断;
(2)因为CCl4沸点为76.8℃,温度比较低,因此保证稳定的CCl4气流,可以通过水浴加热来控制其流量;
(3)氮气不能氧化三氯化铬且充入氮气能使反应物进入管式炉中进行反应;
(4)①利用Na2S2O3滴定生成I2,I2遇淀粉显蓝色;滴入最后一滴时,如果溶液颜色在半分钟内不变色,则达到滴定终点;
若滴定时振荡不充分,刚看到局部变色就停止滴定,则会使样品中无水三氯化铬的质量分数的测量结果偏低;
②溶液中有溶解的氧气,氧气可以氧化I-氧化;
③Cr2O72-和I-发生氧化还原生成碘单质和铬离子;
④由Cr元素守恒及方程式可得关系式2Cr3++~Cr2O72-~3I2~6Na2S2O3,根据关系式计算.
解答 解:根据流程图知,重铬酸铵分解产生的三氧化二铬(Cr2O3难溶于水)、氮气和水,然后洗涤、烘干得到Cr2O3,在加热条件下,在反应器中发生反应Cr2O3+3CCl4═2CrCl3+3COCl2,三氯化铬易升华,在高温下能被氧气氧化,为防止三氯化铬被氧化,通入氮气,且充入的氮气能使反应物进入管式炉中进行反应;最后得到无水三氯化铬;
(1)因为(NH4)2Cr2O7显桔红色,最后一次洗涤的流出液呈无色,说明洗涤干净,
故答案为:最后一次洗涤的流出液呈无色;
(2)因为CCl4沸点为76.8℃,温度比较低,因此保证稳定的CCl4气流,可以通过水浴加热来控制其流量,并用温度计指示温度,
故答案为:水浴加热(并用温度计指示温度);
(3)氮气不能氧化三氯化铬且充入氮气能使反应物进入管式炉中进行反应,为防止三氯化铬被氧化且使反应物进入管式炉中进行反应,充入氮气,
故答案为:赶尽反应装置中的氧气;鼓气使反应物进入管式炉中进行反应;
(4)①利用Na2S2O3滴定生成I2,I2遇淀粉显蓝色,所以可以用淀粉作指示剂;滴入最后一滴时,如果溶液颜色在半分钟内不变色,则达到滴定终点;
若滴定时振荡不充分,刚看到局部变色就停止滴定,则会使样品中无水三氯化铬反应不完全,所以导致它的质量分数的测量结果偏低;
故答案为:淀粉;最后一滴滴入时,蓝色恰好完全褪去,且半分钟内不恢复原色;偏低;
②溶液中有溶解的氧气,氧气可以氧化I-氧化,若不除去其中溶解的氧气使生成的I2的量增大,产生偏高的误差,故加热煮沸,其主要原因是:除去其中溶解的氧气,防止氧气将I-氧化,产生偏高的误差,
故答案为:除去其中溶解的氧气,防止氧气将I-氧化,产生偏高的误差;
③Cr2O72-和I-发生氧化还原生成碘单质和铬离子,离子方程式为:Cr2O72-+6I-+14H+═2Cr3++3I2+7H2O,
故答案为:Cr2O72-+6I-+14H+═2Cr3++3I2+7H2O;
④设25.00mL溶液中n(Cr3+),由Cr元素守恒及方程式可得关系式:2Cr3++~Cr2O72-~3I2~6Na2S2O3,
2Cr3++~Cr2O72-~3I2~6Na2S2O3,
2 6
n(Cr3+) 0.0250mol/L×0.021L
故n(Cr3+)=0.0250mol/L×0.021L×$\frac{1}{3}$=0.000175mol,所以250mL溶液中n′(Cr3+)=0.000175mol×$\frac{250mL}{25mL}$=0.00175mol,根据Cr元素守恒可知n(CrCl3)=n′(Cr3+)=0.00175mol,所以样品中m(CrCl3)=0.00175mol×158.5g/mol=0.2774g,故样品中无水三氯化铬的质量分数为:$\frac{0.2774g}{0.3000g}$×100%=92.5%,
故答案为:92.5%.
点评 本题考查学生对的实验方案原理的理解与评价、物质组成含量的测定、滴定应用、化学计算等,题目难度较大,明确实验原理为解答关键,难点是(4)题计算,易错点是基本实验操作,试题主要考察学生的实验设计能力和计算能力.

①铜与浓硫酸 ②二氧化硅与NaOH溶液 ③铜与浓硝酸 ④石英与纯碱 ⑤铁与液氧 ⑥一氧化氮与氧气 ⑦硅与氧气.
| A. | ①②③⑥ | B. | ②③⑤⑥ | C. | ①④⑤⑦ | D. | ①②③⑦ |
②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H2=-57.3kJ/mol.
下列结论正确的是( )
| A. | 碳的燃烧热用△H3表示,则△H3<△H1 | |
| B. | 碳的燃烧热用△H3表示,则△H3>△H1 | |
| C. | 浓硫酸与稀NaOH溶液反应的中和热值为57.3kJ/mol | |
| D. | 稀醋酸与稀NaOH溶液反应生成1mol水,放出的热量57.3KJ |
| A. | 医用酒精是指质量分数为75%的乙醇溶液 | |
| B. | 用过滤的方法可以分离乙酸乙酯和乙酸 | |
| C. | 葡萄糖、氨基酸在一定条件下都能发生酯化反应 | |
| D. | 在蛋白质溶液中加入浓的无机盐(如(NH4)2SO4、CuSO4等),可使蛋白质的溶解度降低而析出,这个过程称之为变性 |
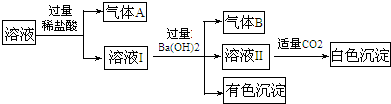
下列判断正确的是( )
| A. | 气体B一定是NH3 | |
| B. | 白色沉淀一定是Al(OH)3 | |
| C. | 溶液中一定存在Al3+、Fe2+、NH4+、NO3- | |
| D. | 溶液中一定不存在大量的Na+ |
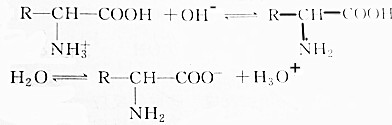
| A. | 增大溶液的pH,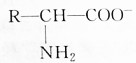 浓度减小 浓度减小 | |
| B. | 降低溶液的pH,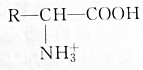 浓度减小 浓度减小 | |
| C. | 如溶液的pH适当,两种氨基酸离子的浓度可能相同 | |
| D. | pH改变,对电离方式无影响 |
| A. | 40.625 | B. | 42.15 | C. | 38.225 | D. | 42.625 |
 .
. ABCDE五种溶液分别是NaOH溶液、氨水、醋酸、盐酸、NH4HSO4溶液的一种.常温下进行下列实验:
ABCDE五种溶液分别是NaOH溶液、氨水、醋酸、盐酸、NH4HSO4溶液的一种.常温下进行下列实验: