题目内容
19.能正确表示下列反应的离子方程式是( )| A. | 硫酸铝溶液中加入过量氨水:Al3++4OH-═AlO2-+2H2O | |
| B. | 浓盐酸与铁屑反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 钠与CuSO4溶液反应:2Na+Cu2+═Cu↓+2Na+ | |
| D. | 在8.12天津大爆炸中消防员喷洒双氧水以防止氰化钠污染环境:CN-+H2O2+H2O═HCO3-+NH3↑ |
分析 A.不符合反应客观事实;
B.不符合反应客观事实;
C.钠与硫酸铜溶液反应生成氢氧化铜沉淀、硫酸钠和氢气;
D.过氧化氢具有强的氧化性能够氧化氰化钠.
解答 解:A.二者反应生成硫酸铵、氢氧化铝沉淀和水,离子方程式:Al3++3NH3•H2O═Al(OH)3↓+3NH4+,故A错误;
B.浓盐酸与铁屑反应生成二价铁离子和氢气,离子方程式:Fe+2H+═Fe2++H2↑,故 B错误;
C.钠与硫酸铜溶液反应的离子反应为2Na+2H2O+Cu2+=Cu(OH)2↓+H2↑+2Na+,故C错误;
D.在8.12天津大爆炸中消防员喷洒双氧水以防止氰化钠污染环境,离子方程式:CN-+H2O2+H2O═HCO3-+NH3↑,故D正确;
故选:D.
点评 本题考查离子反应方程式的书写,明确发生的化学反应及离子反应的书写方法即可解答,注意离子反应遵循客观事实,题目难度不大.

练习册系列答案
相关题目
10.一种锌/铁液流贮能电池结构如图所示.下列说法正确的是( )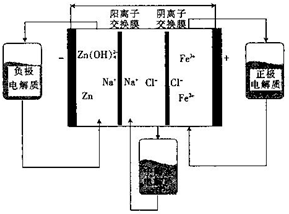

| A. | 放电时,Na+从中间室进入负极室 | |
| B. | 充电时,Cl-从阳极室进入中间室 | |
| C. | 放电时,负极的电极反应为Zn+4OH--2e-=Zn(OH)42- | |
| D. | 充电时,阳极的电极反应为Fe3++e-=Fe2+ |
7.已知反应:①101kPa时,2C(s)+O2(g)═2CO(g)△H1=-221kJ/mol
②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H2=-57.3kJ/mol.
下列结论正确的是( )
②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H2=-57.3kJ/mol.
下列结论正确的是( )
| A. | 碳的燃烧热用△H3表示,则△H3<△H1 | |
| B. | 碳的燃烧热用△H3表示,则△H3>△H1 | |
| C. | 浓硫酸与稀NaOH溶液反应的中和热值为57.3kJ/mol | |
| D. | 稀醋酸与稀NaOH溶液反应生成1mol水,放出的热量57.3KJ |
14.H2和I2在一定条件下能发生反应:H2(g)+I2(g)?2HI(g)△H=-akJ/mol
已知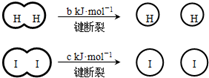 (a、b、c均大于零)
(a、b、c均大于零)
下列说法正确的是( )
已知
 (a、b、c均大于零)
(a、b、c均大于零)下列说法正确的是( )
| A. | H2、I2和HI分子中的化学键都是非极性共价键 | |
| B. | 断开2mol HI分子中的化学键所需能量约为(c+b+a)kJ | |
| C. | 相同条件下,1mol H2(g)和1mol I2(g)总能量小于2molHI(g)的总能量 | |
| D. | 向密闭容器中加入2mol H2(g)和2mol I2(g),充分反应后放出的热量小于2a kJ |
11.下列说法正确的是( )
| A. | 医用酒精是指质量分数为75%的乙醇溶液 | |
| B. | 用过滤的方法可以分离乙酸乙酯和乙酸 | |
| C. | 葡萄糖、氨基酸在一定条件下都能发生酯化反应 | |
| D. | 在蛋白质溶液中加入浓的无机盐(如(NH4)2SO4、CuSO4等),可使蛋白质的溶解度降低而析出,这个过程称之为变性 |
8.氨基酸在溶液中按两种方式电离以下判断正确的是( )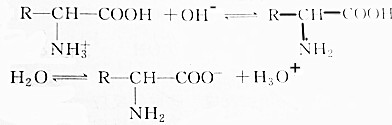
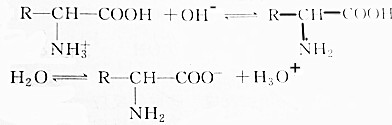
| A. | 增大溶液的pH,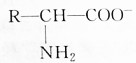 浓度减小 浓度减小 | |
| B. | 降低溶液的pH,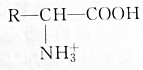 浓度减小 浓度减小 | |
| C. | 如溶液的pH适当,两种氨基酸离子的浓度可能相同 | |
| D. | pH改变,对电离方式无影响 |
12.下列叙述错误的是( )
| A. | 把aL0.1mol/L的CH3COOH溶液与bL0.1mol/L的KOH溶液混合,所得溶液中一定存在:c(K+)+c(H+)═c(CH3COO-)+c(OH-) | |
| B. | 把0.1mol/L的NaHCO3溶液与0.3mol/L的Ba(OH)2溶液等体积混合,所得溶液中一定存在:c(OH-)>c(Ba+)>c(Na+)>c(H+) | |
| C. | 向1mol/L的CH3COOH溶液中加入少量CH3COONa固体,由于CH3COONa水解显碱性,所以溶液的pH升高 | |
| D. | 常温下,在pH=3的CH3COOH溶液和pH=11的NaOH溶液中,水的电离程度相同. |

 .
.