题目内容
有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B-少一个电子层,B原子得一个电子填入3p轨道后,3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等子中子数.R是由A、D两元素形成的离子化合物,其中A+与D2-离子数之比为2:1.请回答下列问题:
(1)R形成的晶体属于 (填写离子、分子、原子)晶体.
(2)C3-的电子排布式为 ,在CB3分子中C元素原子的原子轨道发生的是 杂化,CB3分子的VSEPR模型为 .
(3)C的氢化物在水中的溶解度特别大,原因
(4)D元素与同周期相邻元素的第一电离能由大到小的关系是: (用元素符号表示);用一个化学方程式说明B、D两元素形成的单质的氧化性强弱: .
(5)已知下列数据:
4Cu(s)+O2(g)═2Cu2O(s)△H=-337.2kJ?mol-1
2Cu(s)+O2(g)═2CuO(s)△H=-314.6kJ?mol-1
由Cu2O和O2反应生成CuO的热化学方程式是 .
(1)R形成的晶体属于
(2)C3-的电子排布式为
(3)C的氢化物在水中的溶解度特别大,原因
(4)D元素与同周期相邻元素的第一电离能由大到小的关系是:
(5)已知下列数据:
4Cu(s)+O2(g)═2Cu2O(s)△H=-337.2kJ?mol-1
2Cu(s)+O2(g)═2CuO(s)△H=-314.6kJ?mol-1
由Cu2O和O2反应生成CuO的热化学方程式是
考点:位置结构性质的相互关系应用,原子核外电子排布,元素电离能、电负性的含义及应用,热化学方程式
专题:化学反应中的能量变化,元素周期律与元素周期表专题,化学键与晶体结构
分析:B原子得一个电子填入3p轨道后,3p轨道已充满,B为Cl元素;A+比B-少一个电子层,则A为Na;C原子的p轨道中有3个未成对电子,C原子的外围电子排布为ns2np3,是第ⅤA族元素,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大,所以为N元素;D的最高化合价和最低化合价的代数和为4,为第ⅥA族元素,最高价氧化物中含D的质量分数为40%,可推知D的相对原子质量为32,其核内质子数等于中子数,所以质子数为16,D为S元素;A+是Na+离子,D2-离子是S2-离子,R是由Na+离子与S2-离子以2:1形成的离子化合物,R是硫化钠,据此解答.
解答:
解:B原子得一个电子填入3p轨道后,3p轨道已充满,B为Cl元素;A+比B-少一个电子层,则A为Na;C原子的p轨道中有3个未成对电子,C原子的外围电子排布为ns2np3,是第ⅤA族元素,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大,所以为N元素;D的最高化合价和最低化合价的代数和为4,为第ⅥA族元素,最高价氧化物中含D的质量分数为40%,可推知D的相对原子质量为32,其核内质子数等于中子数,所以质子数为16,D为S元素;A+是Na+离子,D2-离子是S2-离子,R是由Na+离子与S2-离子以2:1形成的离子化合物,R是硫化钠,
(1)R是由Na、S两元素形成的离子化合物,属于离子晶体,故答案为:离子;
(2)N3-核外有10个电子,根据构造原理知,该离子基态核外电子排布式为:ls22s22p6,CB3分子为NCl3分子,N原子有一对孤对电子,与Cl原子成3个σ键,N原子产生sp3杂化,所以NCl3分子的VSEPR模型为四面体形,
故答案为:ls22s22p6;sp3;四面体形;
(3)氨分子和水分子间可以形成氢键,且氨分子和水分子均为极性分子,相似相溶,氨分子和水分子还可以发生反应,氨气极易溶于水,
故答案为:氨分子和水分子间可以形成氢键,且氨分子和水分子均为极性分子,相似相溶,氨分子和水分子还可以发生反应,氨气极易溶于水;
(4)同一周期元素中,元素的第一电离能随着原子序数的增大而呈增大趋势,但第VA族元素第一电离能大于相邻元素,所以P、S、Cl元素的第一电离能大小顺序是:Cl>P>S;
同一周期元素中,元素的电负性随着原子序数的增大而增大,一般来说电负性越强,元素的非金属性越强,对应的单质的氧化性越强,如在H2S+Cl2=2HCl+S↓反应中,Cl2的氧化性大于O2的氧化性,
故答案为:Cl>P>S;H2S+Cl2=2HCl+S↓;
(5)已知:①4Cu(s)+O2(g)═2Cu2O(s)△H=-337.2kJ?mol-1
②2Cu(s)+O2(g)═2CuO(s)△H=-314.6kJ?mol-1
根据盖斯定律,②×2-①得:2Cu2O(s)+O2(g)=4CuO(s)△H=-292.0kJ?mol-1,
故答案为:2Cu2O(s)+O2(g)=4CuO(s)△H=-292.0kJ?mol-1.
(1)R是由Na、S两元素形成的离子化合物,属于离子晶体,故答案为:离子;
(2)N3-核外有10个电子,根据构造原理知,该离子基态核外电子排布式为:ls22s22p6,CB3分子为NCl3分子,N原子有一对孤对电子,与Cl原子成3个σ键,N原子产生sp3杂化,所以NCl3分子的VSEPR模型为四面体形,
故答案为:ls22s22p6;sp3;四面体形;
(3)氨分子和水分子间可以形成氢键,且氨分子和水分子均为极性分子,相似相溶,氨分子和水分子还可以发生反应,氨气极易溶于水,
故答案为:氨分子和水分子间可以形成氢键,且氨分子和水分子均为极性分子,相似相溶,氨分子和水分子还可以发生反应,氨气极易溶于水;
(4)同一周期元素中,元素的第一电离能随着原子序数的增大而呈增大趋势,但第VA族元素第一电离能大于相邻元素,所以P、S、Cl元素的第一电离能大小顺序是:Cl>P>S;
同一周期元素中,元素的电负性随着原子序数的增大而增大,一般来说电负性越强,元素的非金属性越强,对应的单质的氧化性越强,如在H2S+Cl2=2HCl+S↓反应中,Cl2的氧化性大于O2的氧化性,
故答案为:Cl>P>S;H2S+Cl2=2HCl+S↓;
(5)已知:①4Cu(s)+O2(g)═2Cu2O(s)△H=-337.2kJ?mol-1
②2Cu(s)+O2(g)═2CuO(s)△H=-314.6kJ?mol-1
根据盖斯定律,②×2-①得:2Cu2O(s)+O2(g)=4CuO(s)△H=-292.0kJ?mol-1,
故答案为:2Cu2O(s)+O2(g)=4CuO(s)△H=-292.0kJ?mol-1.
点评:本题考查了物质结构和性质,题目较为综合,涉及核外电子排布、杂化轨道、分子结构、氢键、元素周期律、热化学方程式等,推断元素的种类是正确解答的关键.

练习册系列答案
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
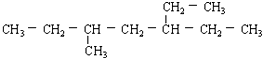 含有一个双键的烯烃,氢化后的产物结构简式为此烃可能有的结构有( )
含有一个双键的烯烃,氢化后的产物结构简式为此烃可能有的结构有( )| A、4种 | B、5种 | C、6种 | D、7种 |
实验是研究化学的基础,下图中所示的实验方法、装置或操作完全正确的是( )
A、 检查装置气密性 检查装置气密性 |
B、 加热溶液 加热溶液 |
C、 铁丝在氧气中燃烧 铁丝在氧气中燃烧 |
D、 称量 称量 |