题目内容
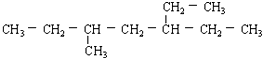 含有一个双键的烯烃,氢化后的产物结构简式为此烃可能有的结构有( )
含有一个双键的烯烃,氢化后的产物结构简式为此烃可能有的结构有( )| A、4种 | B、5种 | C、6种 | D、7种 |
考点:同分异构现象和同分异构体
专题:同系物和同分异构体
分析:根据加成反应原理采取逆推法还原C=C双键,烷烃分子中相邻碳原子上均含有氢原子的碳原子间是对应烯烃存在C=C的位置,还原双键时注意防止重复.
解答:
解:根据烯烃与H2加成反应的原理,推知该烷烃分子中相邻碳原子上均含有原子的碳原子间是对应烯烃存在C=C的位置,该烷烃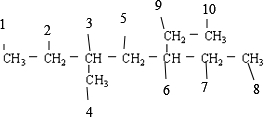
中能形成双键键位置有:1和2之间、2和3之间、3和4之间、3和5之间、5和6之间、6和7之间(6和9)、7和8之间(9和10),故该烯烃共有7种,
故选D.

中能形成双键键位置有:1和2之间、2和3之间、3和4之间、3和5之间、5和6之间、6和7之间(6和9)、7和8之间(9和10),故该烯烃共有7种,
故选D.
点评:本题考查了加成反应的运用以及同分异构体的书写,理解加成反应原理是解题的关键,采取逆推法还原C=C双键,注意分析分子结构防止重写、漏写.

练习册系列答案
相关题目
在RNH2?H2O?RNH3++OH-的平衡中,要使RNH2?H2O的电离程度及c(OH-)都增大,可采取的措施是( )
| A、通入HCl | B、加少量NaOH固体 |
| C、加水 | D、升温 |
0.02mol的铝单质在氧气中完全燃烧,燃烧的产物与2.00mol/L的盐酸反应.若要反应完全,则最少需要多少毫升的盐酸( )
| A、15cm3 |
| B、20cm3 |
| C、30cm3 |
| D、60cm3 |
下列离子方程式书写正确的是( )
| A、向CaCl2溶液中通入少量CO2气体:Ca2++CO2+H2O=CaCO3↓+2H+ |
| B、碳酸钠溶液与硫酸氢钠溶液反应:HCO3-+H+=CO2↑+H2O |
| C、向Ba(OH)2溶液中滴加NH4HSO4溶液至刚好沉淀完全:Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3?H2O+H2O |
| D、含有FeBr2溶液中通入足量的Cl2:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
下列离子方程式正确的是( )
| A、FeCl2溶液中通入Cl2:Fe2++Cl2=Fe3++2Cl- |
| B、向氯化铝溶液中加入足量氨水:Al3++4NH3?H2O=AlO2-+2H2O+4NH4+ |
| C、Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
| D、少量CO2气体通入苯酚钠溶液中:C6H5O-+CO2+H2O=C6H5OH+HCO3- |
下列各组离子在溶液中一定能够大量共存的是( )
| A、在含有大量OH-的溶液中:NO3-、Na+、Cl-、AlO2- |
| B、在强酸性溶液中:K+、HCO3-、SO42- |
| C、在含有大量SO42-的溶液中:Mg2+、Na+、Cu2+、Cl- |
| D、在含有大量Fe2+的溶液中:H+、Na+、Cl-、NO3- |
下列离子方程式正确的是( )
| A、过氧化钠加入水中:2O22-+2H2O═4OH-+O2↑ | ||
B、碳酸氢钠溶液加入盐酸:CO
| ||
| C、氢氧化铜中加入盐酸:OH-+H+═H2O | ||
| D、四氧化三铁跟稀硫酸反应:Fe3O4+8H+═Fe2++2Fe3++4H2O |