题目内容
下列关于Na2O与Na2O2的说法中,错误的是( )
| A、两者颜色不同 |
| B、均可与H2O、CO2反应 |
| C、Na2O能被氧化成Na2O2 |
| D、它们的固体溶于水滴加酚酞试液后,现象相同 |
考点:钠的重要化合物
专题:元素及其化合物
分析:A、氧化钠是白色的,过氧化钠是黄色的固体;
B、氧化钠是碱性氧化物,具有碱性氧化物通性.过氧化钠与水反应生成氢氧化钠,与CO2反应生成碳酸钠和氧气;
C、由于钠在常温下与氧气反应生成氧化钠,在加热情况下生成过氧化钠,可知氧化钠易被氧化为过氧化钠;
D、氧化钠是碱性氧化物,溶于水滴加酚酞试液后变红;过氧化钠除了与水反应生成氢氧化钠,过氧化钠还具有具有强氧化性而漂白,所以溶于水滴加酚酞试液后先变红后退色;
B、氧化钠是碱性氧化物,具有碱性氧化物通性.过氧化钠与水反应生成氢氧化钠,与CO2反应生成碳酸钠和氧气;
C、由于钠在常温下与氧气反应生成氧化钠,在加热情况下生成过氧化钠,可知氧化钠易被氧化为过氧化钠;
D、氧化钠是碱性氧化物,溶于水滴加酚酞试液后变红;过氧化钠除了与水反应生成氢氧化钠,过氧化钠还具有具有强氧化性而漂白,所以溶于水滴加酚酞试液后先变红后退色;
解答:
解:A、氧化钠是白色的,但是过氧化钠是黄色的固体,故A正确;
B、氧化钠是碱性氧化物,能与水、酸性氧化物反应,与水反应生成氢氧化钠,二氧化碳是酸性氧化物,与氧化钠反应生成碳酸钠;过氧化钠与水反应生成氢氧化钠,与CO2反应生成碳酸钠和氧气,故B正确;
C、因2Na2O+O2═Na2O2,则Na2O能被氧化成Na2O2,故C正确;
D、氧化钠是碱性氧化物,溶于水滴加酚酞试液后变红;过氧化钠除了与水反应生成氢氧化钠,过氧化钠还具有具有强氧化性而漂白,所以溶于水滴加酚酞试液后先变红后退色,故D错误;
故选:D.
B、氧化钠是碱性氧化物,能与水、酸性氧化物反应,与水反应生成氢氧化钠,二氧化碳是酸性氧化物,与氧化钠反应生成碳酸钠;过氧化钠与水反应生成氢氧化钠,与CO2反应生成碳酸钠和氧气,故B正确;
C、因2Na2O+O2═Na2O2,则Na2O能被氧化成Na2O2,故C正确;
D、氧化钠是碱性氧化物,溶于水滴加酚酞试液后变红;过氧化钠除了与水反应生成氢氧化钠,过氧化钠还具有具有强氧化性而漂白,所以溶于水滴加酚酞试液后先变红后退色,故D错误;
故选:D.
点评:本题考查钠的氧化物,明确发生的化学反应及相关的概念是解答本题的关键,难度不大.

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目
下列关于MgO和Al2O3性质和用途的说法不符合事实的是( )
| A、都可与盐酸反应 |
| B、都难溶于水 |
| C、都常用作耐火材料 |
| D、都可与氢氧化钠溶液反应 |
根据有机化合物的命名原则,下列命名正确的是( )
A、 3-甲基-1?3-丁二烯 |
B、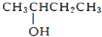 2-羟羟基丁烷 |
C、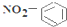 硝基苯 |
D、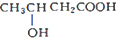 3-羟基丁酸 |
主族元素M、R形成的简单离子M2-离子与R+离子的核外电子数之和为20,下列说法正确的是( )
| A、M与R的原子序数之差可能等于7 |
| B、若M在第3周期,则R一定在第2周期 |
| C、M2-的离子半径可能比R+的离子半径小 |
| D、两种离子结合形成的化合物可能是共价化合物 |
实验室中金属钠保存在煤油中,若将一小块金属钠露置于空气中发生一系列变化,最终产物是( )
| A、NaOH |
| B、Na2O |
| C、Na2O2 |
| D、Na2CO3 |
下列比较正确的是( )
| A、第一电离能:I1(P)>I1(S) |
| B、离子半径:r(Al3+)>r(O2-) |
| C、能量:E(4s)>E(3d) |
| D、电负性:K元素>Na元素 |
下列各组物质中,前者为强电解质,后者为弱电解质的是( )
| A、氯化钠,浓氨水 |
| B、氢氧化钠,水 |
| C、硫酸,硫酸钡 |
| D、氯化银,二氧化硫 |
设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A、1 mol?L-1NaCl溶液中含有Cl-的个数为NA |
| B、5.6g金属铁与盐酸反应失去的电子数为0.2NA |
| C、标准状况下,22.4L的水中含有的原子数为3NA |
| D、常温常压下,11.2L氯气中所含的原子数为NA |