题目内容
设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A、1 mol?L-1NaCl溶液中含有Cl-的个数为NA |
| B、5.6g金属铁与盐酸反应失去的电子数为0.2NA |
| C、标准状况下,22.4L的水中含有的原子数为3NA |
| D、常温常压下,11.2L氯气中所含的原子数为NA |
考点:阿伏加德罗常数
专题:
分析:A、溶液体积不明确;
B、依据n=
算物质的量,结合铁与盐酸反应生成氯化亚铁来分析;
C、标况下,水为液态;
D、常温常压下,气体摩尔体积大于22.4L/mol.
B、依据n=
| m |
| M |
C、标况下,水为液态;
D、常温常压下,气体摩尔体积大于22.4L/mol.
解答:
解:A、溶液体积不明确,无法计算的Cl-的个数,故A错误;
B、5.6 g铁物质的量为0.1mol,与足量的盐酸反应失去电子数为0.2 NA,故B正确;
C、标况下,水为液态,故C错误;
D、常温常压下,气体摩尔体积大于22.4L/mol,故11.2L氯气的物质的量小于0.5mol,即含有的原子的个数小于NA个,故D错误.
故选B.
B、5.6 g铁物质的量为0.1mol,与足量的盐酸反应失去电子数为0.2 NA,故B正确;
C、标况下,水为液态,故C错误;
D、常温常压下,气体摩尔体积大于22.4L/mol,故11.2L氯气的物质的量小于0.5mol,即含有的原子的个数小于NA个,故D错误.
故选B.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
下列关于Na2O与Na2O2的说法中,错误的是( )
| A、两者颜色不同 |
| B、均可与H2O、CO2反应 |
| C、Na2O能被氧化成Na2O2 |
| D、它们的固体溶于水滴加酚酞试液后,现象相同 |
两个体积相同的容器,一个盛有NO,一个盛有N2和O2,在同温同压下两容器内的气体一定具有相同的( )
| A、原子总数 | B、质子总数 |
| C、密度 | D、质量 |
设阿伏加德罗常数的值为NA,则下列说法不正确的是( )
| A、15g甲基(-CH3)所含有的电子数是9NA |
| B、常温常压下,26g苯乙烯和苯组成的混合物中所含有的原子数为4NA |
| C、常温常压下,1molCnH2n+2所含有的共价键数目为(3n+1)NA |
| D、标准状况下,1L辛烷充分燃烧后生成的气态产物的分子数为8/22.4 NA |
用NA表示阿伏加德罗常数的值.下列叙述中正确的是( )
A、D
| ||
| B、相同物质的量的OH-和CH3+含有相同数目的电子 | ||
| C、NA个H2分子与0.5 NA个CO分子所占的体积比一定是2:1 | ||
| D、25℃时,pH=1的H2SO4溶液中含有H+的数目为0.2NA |
化学兴趣小组设计如图实验装置.电解开始不久,铜电极附近溶液为无色,过了相当长时间后才呈蓝紫色.下列有关描述正确的是( )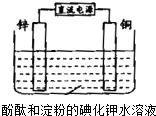

| A、电子由锌极流向铜极 |
| B、锌电极上的电极反应为:4OH--4e-═2H2O+O2↑ |
| C、铜电极实验现象的原因是生成的Cu2+和I-发生了反应 |
| D、将铜换成铁,电解开始后不久铁电极附近溶液即呈蓝紫色 |