题目内容
8.硫酸是一种重要的化工产品,硫酸的消耗量常被视为一个国家工业发展水平的一种标志.目前的重要生产方法是“接触法”,有关接触氧化反应2SO2+O2$?_{500℃}^{催化剂}$ 2SO3,的说法不正确的是( )| A. | 该反应为可逆反应,故在一定条件下二氧化硫和氧气不可能全部转化为三氧化硫 | |
| B. | 达到平衡后,反应就停止了,故此时正、逆反应速率相等且均为零 | |
| C. | 一定条件下,向某密闭容器中加入2molSO2和1molO2,则从反应开始到达到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,某一时刻,正、逆反应速率相等 | |
| D. | 在利用上述反应生产三氧化硫时,要同时考虑反应所能达到的限度和化学反应速率两方面的问题 |
分析 A、依据可逆反应的特征分析判断;
B、化学平衡是动态平衡,正反应速率和逆反应速率相同;
C、依据平衡建立的过程分析;
D、合成需要考虑温度压强对平衡的影响和经济效益.
解答 解:A、可逆反应是在一定条件下不能进行彻底的反应,正反应和逆反应同时进行,该反应为可逆反应,故在一定条件下SO2和O2不可能全部转化为SO3 ,故A正确;
B、达到平衡后,正反应速率和逆反应速率相同,是动态平衡,速率不能为0,故B错误;
C、一定条件下,向某密闭容器中加入2 mol SO2和1 mol O2,则从反应开始到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,某一时刻,正、逆反应速率相等达到平衡,故C正确;
D、反应是放热反应,但为了反应速率需要一定温度,催化剂活性最大,压强在常温下,二氧化硫的转化率已经横高改变压强对转化率影响不大,故D正确;
故选B.
点评 本题考查了化学平衡的建立和平衡的特征分析,注意平衡建立过程、平衡的可逆性理解是解题关键,题目难度中等.

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案
相关题目
19.一定温度下在一个2L的密闭容器中发生反应4A(s)+3B(g)?2C(g)+D(g),经2min达平衡状态,此时B反应消耗了0.9mol,下列说法正确的是( )
| A. | 平衡状态时A、B、C、D的反应速率均为0 | |
| B. | C的平均反应速率为:0.15mol/(L•min) | |
| C. | 充入N2使压强增大可加快反应速率 | |
| D. | 此时,V(A):V(B):V(C):V(D)=4:3:2:1 |
16.某溶液中可能含有I-、NH4+、Cu2+、SO32-,向溶液中加入足量的溴水,反应后溶液仍呈无色,则下列关于溶液组成的判断正确的是( )
| A. | 肯定不含I- | B. | 肯定不含NH4+ | C. | 肯定不含Cu2+ | D. | 肯定不含SO32- |
13.下列有关离子方程式的书写正确的是( )
| A. | NaHCO3溶液和盐酸;CO32-+2H+═H2O+CO2↑ | |
| B. | 在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3═2FeO42-+3Cl-+H2O+4H+ | |
| C. | 向硫化钠溶液中滴入氯化铝溶液:2Al3++3S2-═Al2S3↓ | |
| D. |  溶液通入少量CO2: 溶液通入少量CO2: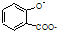 +CO2+H2O→ +CO2+H2O→ +HCO3- +HCO3- |
17.阿伏加德罗常数的准确值是( )
| A. | 12g12C所含有的碳原子数 | B. | 1mol水中电子数 | ||
| C. | 6.02×1023 | D. | 6.02×10-23 |
18.物质的量浓度相同的下列溶液中,符合按pH由小到大排列的是( )
| A. | K2CO3 KHCO3 KCl NH4Cl | |
| B. | K2CO3 KHCO3 NH4Cl KCl | |
| C. | (NH4)2SO4 NH4Cl KNO3 K2CO3 | |
| D. | NH4Cl (NH4)2SO4 K2CO3 KNO3 |
 0.9 mol·L-1,当加入2 mol·L-1的KOH溶液100mL时,生成沉淀恰好溶解,则原混合物中K+的物质的量浓度是
0.9 mol·L-1,当加入2 mol·L-1的KOH溶液100mL时,生成沉淀恰好溶解,则原混合物中K+的物质的量浓度是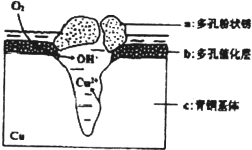 我国古代青铜器工艺精湛,有很高的艺术价值和历史价值,但出土的青铜器因受到环境腐蚀,欲对其进行修复和防护具有重要意义.
我国古代青铜器工艺精湛,有很高的艺术价值和历史价值,但出土的青铜器因受到环境腐蚀,欲对其进行修复和防护具有重要意义.
 CH3COOC2H5+H2O,该反应的类型为酯化反应(或取代反应);
CH3COOC2H5+H2O,该反应的类型为酯化反应(或取代反应); ;D的一种同分异构体的结构简式为CH3CHO.
;D的一种同分异构体的结构简式为CH3CHO.