题目内容
13.下列各组物质不属于同分异构体的是( )| A. | 乙苯和1,2二甲苯 | B. | 邻氯甲苯和对氯甲苯 | ||
| C. | 2甲基丁烷和戊烷 | D. | 乙醇和丙醇 |
分析 分子式相同,结构不同的化合物互为同分异构体,据此解题.
解答 解:A.1,2二甲苯和乙苯是分子式都为C8H10,结构不同的化合物,互为同分异构体,故A不选;
B.邻氯甲苯和对氯甲苯分子式都为C7H7Cl,结构不同,互为同分异构体,故B不选;
C.2-甲基丁烷和戊烷都属于戊烷的同分异构体,属于同分异构体,故D不选;
D.乙醇和丙醇的分子式分别为C2H6O、C3H8O,分子式不同,不属于同分异构体,故D选.
故选D.
点评 本题考查同分异构体的概念与区别,难度不大,关键是根据名称写出分子式进行判断.

练习册系列答案
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案
相关题目
15.乙烯的相关转化关系如图.下列有关说法正确的是( )
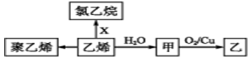

| A. | 甲与CH3OCH3互为同分异构体 | B. | X为Cl2 | ||
| C. | 聚乙烯是纯净物 | D. | 甲→乙反应类型为取代反应 |
4.T1℃时.在2L的密闭容器中,反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0达到平衡,反应过程中部分数据见下表.下列说法正确的是( )
| 反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) | |
| 反应I 恒温恒容 | 0min | 2 | 6 | 0 | 0 |
| 10min | 4.5 | ||||
| 20min | 1 | ||||
| 30min | 1 | ||||
| 反应Ⅱ 绝热恒容 | 0min | 0 | 0 | 2 | 2 |
| A. | 达到平衡时,反应Ⅰ、Ⅱ对比,平衡常数:K(Ⅰ)>K(Ⅱ) | |
| B. | 对于反应Ⅰ,前10min内的平均反应速率v(CH3OH)=0.025mol•L-1•min-1 | |
| C. | 对于反应Ⅰ,若30min时只改变温度为T2℃,再次达到平衡时H2的物质的量为3.2mol,则T1>T2 | |
| D. | 对于反应Ⅰ,若30min时只向容器中再充入1molCO2(g)和1molH2O(g),则平衡正向移动 |
8.下列生活中的问题,不能用金属晶体结构加以解释的是( )
| A. | 铁易生锈 | B. | 用金属铝制成导线 | ||
| C. | 用金箔做外包装 | D. | 用铁制品做炊具 |
18.已知NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 常温常压下,0.1NA个NH3分子的质量为1.7g | |
| B. | 标准状况下,1mol氟化氢的体积为22.4L | |
| C. | 2.4g金属镁转化为镁离子时失去的电子数目为0.1NA | |
| D. | 1L 1mol/L NaCl溶液中含有的离子总数为NA |
5.有一种盐A和KOH反应,生成有刺激性气味的气体B,B经过一系列氧化再溶于水可得到酸C,B和C反应又可以生成A,则A是( )
| A. | NH4Cl | B. | (NH4)2SO4 | C. | NH4NO3 | D. | NH4NO2 |
2.下列物质属于烃的是( )
| A. | CH4 | B. | H2CO3 | C. | CH3Cl | D. | HCl |
3.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 0.1 mol SO2、O2的混合气体,充分反应达到平衡后体系内氧原子数目为0.2NA | |
| B. | 0.1 mol ${\;}_{38}^{90}$Sr原子中含中子数为3.8NA | |
| C. | 标准状况下,22.4 L空气中单质分子数目为NA | |
| D. | 100 g质量分数是98%的浓硫酸中所含氧原子数为4NA |
