题目内容
2.下列物质属于烃的是( )| A. | CH4 | B. | H2CO3 | C. | CH3Cl | D. | HCl |
分析 分子组成只含有C、H元素的化合物为烃,即属于烃的物质必须只含有碳氢元素,常见的烃有烷烃、烯烃、炔烃、苯及苯的同系物等,据此进行解答.
解答 解:烃分子中只含有C和H元素,不能含有其它元素,选项中H2CO3、CH3Cl和HCl都不属于烃,只有甲烷属于烃类,
故选A.
点评 本题考查了烃的概念及判断,题目难度不大,注意掌握烃的分子组成及性质,明确烃的分类、结构及具有的性质.

练习册系列答案
 小题狂做系列答案
小题狂做系列答案
相关题目
4.短周期主族元素X、Y、Z、W的原子序数依次增大,X、W同主族;Y、Z同周期;X、Y、Z三种元素形成一种化合物M,25℃时,0.1mol•L-1的M溶液中$\frac{c(O{H}^{-})}{c({H}^{+})}$=1.0×10-12.下列说法正确的是( )
| A. | 简单离子半径:Y<Z<W | |
| B. | X分別与Z、W形成的化合物中,所含化学键类型相同 | |
| C. | X、Y形成的最简单化合物的电子式为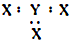 | |
| D. | Z分別与X、W均可形成具有漂白性的化合物 |
13.下列各组物质不属于同分异构体的是( )
| A. | 乙苯和1,2二甲苯 | B. | 邻氯甲苯和对氯甲苯 | ||
| C. | 2甲基丁烷和戊烷 | D. | 乙醇和丙醇 |
10.高铁酸盐在水溶液中有四种含铁型体,25℃时,它们的物质的量分数随pH的变化如图所示,下列叙述错误的是( )

| A. | pH=2.2时,溶液中主要含铁形体浓度的大小关系为c(H3FeO4+)>c(HFeO4-) | |
| B. | 为获得尽可能纯净的高铁酸盐,pH应控制pH≥9 | |
| C. | 常温时,NaHFeO4水溶液显碱性 | |
| D. | 向pH=6的高铁酸盐溶液中加入KOH溶液,发生反应的离子方程式为HFeO4-+OH-═FeO42-+H2O |
17.下列有关有机物的说法正确的是( )
| A. | 1mol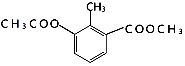 能与4molNaOH充分反应 能与4molNaOH充分反应 | |
| B. | 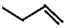 系统命名法为3-丁烯 系统命名法为3-丁烯 | |
| C. | 1mol 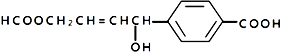 可以与4molH2发生加成 可以与4molH2发生加成 | |
| D. | 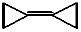 的碳原子都在一个平面内,且它的二氯代物为3种 的碳原子都在一个平面内,且它的二氯代物为3种 |
7.实验室以蛇纹石酸浸出液(主要含Fe3+,还有一定量的Al3+、Mn2+、Ca2+、Mg2+等)为原料制备高纯氧化铁,流程如图1:
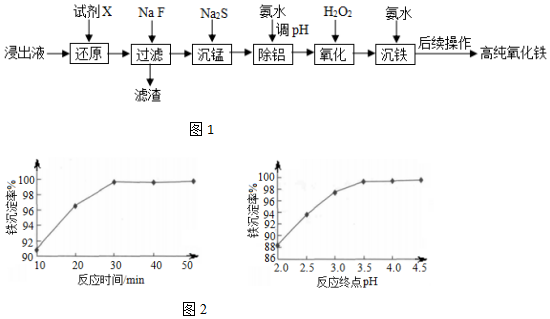
已知流程中相关金属离子生成氢氧化物沉淀的pH如表:
(1)“还原”时,应选择C(填字母).
A.Zn粉 B.NaClO溶液 C.Fe粉
(2)“滤渣”的主要成分除含有少量MnF2外,还含有CaF2、MgF2(填化学式).
(3)“沉锰”时,已知:Ksp(MnS)=4.65×10-14.为确保沉锰完全[即溶液中c(Mn2+)<1.0×10-6 mol•L-1],应保持溶液中c(S2-)>4.65×10-8mol•L-1mol•L-1.
(4)“除铝”时,控制溶液pH的范围为5.0~5.8.
(5)“氧化”时,常用酸性K2Cr2O7溶液检测是否残留未被氧化的金属离子,该反应的离子方程式为Cr2O72-+14H++6Fe2+═2Cr3++6Fe3++7H2O.
(6)“沉铁”时,反应温度为85℃条件下,反应时间和反应终点pH对铁的沉淀率的影响分别如图2所示,则最佳的工艺条件是反应时间30min、终点pH=3.5.

已知流程中相关金属离子生成氢氧化物沉淀的pH如表:
| 氢氧化物 | Fe3+ | Fe2+ | Al3+ |
| 开始沉淀的pH | 1.1 | 5.8 | 3.0 |
| 沉淀完全的pH | 3.2 | 8.8 | 5.0 |
A.Zn粉 B.NaClO溶液 C.Fe粉
(2)“滤渣”的主要成分除含有少量MnF2外,还含有CaF2、MgF2(填化学式).
(3)“沉锰”时,已知:Ksp(MnS)=4.65×10-14.为确保沉锰完全[即溶液中c(Mn2+)<1.0×10-6 mol•L-1],应保持溶液中c(S2-)>4.65×10-8mol•L-1mol•L-1.
(4)“除铝”时,控制溶液pH的范围为5.0~5.8.
(5)“氧化”时,常用酸性K2Cr2O7溶液检测是否残留未被氧化的金属离子,该反应的离子方程式为Cr2O72-+14H++6Fe2+═2Cr3++6Fe3++7H2O.
(6)“沉铁”时,反应温度为85℃条件下,反应时间和反应终点pH对铁的沉淀率的影响分别如图2所示,则最佳的工艺条件是反应时间30min、终点pH=3.5.
14.设NA为阿伏加德罗常数的值.下列有关说法正确的是( )
| A. | 32gCu在足量O2或硫蒸气中完全燃烧失去的电子数均为NA | |
| B. | 4g甲烷和8g甲醇含有的氢原子数均为NA | |
| C. | 标准状况下,5.6L乙烷中含有的共价键数目为1.5NA | |
| D. | 一定条件下,32gSO2与足量O2反应,转移电子数为NA |
11.下列实验现象和结论相对应且正确的是( )
| 选项 | 实验 | 现象 | 结论 |
| A | 用铂丝蘸取少量某溶液进行焰色反应 | 火焰呈黄色 | 证明该溶液中存在Na+、不含K+ |
| B | 用浓盐酸和石灰石反应声生的气体直接通入Na2SiO3溶液中 | Na2SiO3溶液变浑浊 | C元素的非金属性大于Si元素 |
| C | 将石蜡油在碎瓷片上加热,产生的气体通过酸性KMnO4溶液 | 酸性KMnO4溶液紫红色褪去 | 石蜡油分解产生了不同于烷烃的气体,且该气体具有还原性 |
| D | 某溶液加入稀硝酸酸化的BaCl2溶液 | 产生白色沉淀 | 该溶液中一定存在SO42-或者Ag+ |
| A. | A | B. | B | C. | C | D. | D |
5.下列有关“化学与生活”的叙述正确的是( )
| A. | Fe(OH)3胶体无色、透明,能产生丁达尔现象 | |
| B. | 六水氯化钙可用作食品干燥剂 | |
| C. | 雾霾是一种分散系,分散剂是空气,带活性炭口罩防雾霾的原理是吸附原理 | |
| D. | 用含硅胶、铁粉的透气小袋与食品一起密封包装,该过程没有发生化学反应 |