题目内容
16.阿斯巴甜是目前使用最广泛的甜味剂.甜度约为蔗糖的200倍,其结构简式为: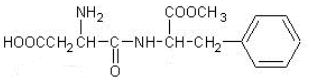
下列关于阿斯巴甜的说法正确的是( )
| A. | 分子式为C14H19N2O5 | B. | 既能与酸反应又能与碱反应 | ||
| C. | 不能发生水解反应 | D. | 1mol该物质最多可与2molNaOH反应 |
分析 由结构简式可知该物质含-COOH、-NH2、-CONH-、-COOC-及苯环结构,结合酯、肽键及氨基酸的性质等来解答.
解答 解:A.由结构简式可知,分子式为C14H17N2O5,故A错误;
B.含-COOH、-NH2,则既能与酸反应又能与碱反应,故B正确;
C.含有酯基,可发生水解反应,故C错误;
D.能与氢氧化钠反应的官能团为羧基,酯基,且肽键水解生成的羧基也可与氢氧化钠反应,则1mol该物质最多可与3molNaOH反应,故D错误.
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重氨基酸性质的考查,选项D为解答的易错点,题目难度中等.

练习册系列答案
 优加精卷系列答案
优加精卷系列答案
相关题目
6.下列实验现象描述不正确的是( )
| 选项 | 实验 | 现象 |
| A | 加热放在坩埚中的小钠块 | 钠先熔化成光亮的小球,燃烧时,火焰为黄色,燃烧后,生成淡黄色固体 |
| B | 在酒精灯上加热铝箔 | 铝箔熔化,失去光泽,熔化的铝并不滴落,好像有一层膜兜着 |
| C | 在含有酚酞的水中加入一小块钠 | 钠浮在水面上,四处游动,发出嘶嘶响声,溶液变红 |
| D | 在空气中久置的铝条放入稀硫酸溶液中 | 立刻产生大量无色气泡,铝条逐渐变细,铝条逐渐发热 |
| A. | A | B. | B | C. | C | D. | D |
8. (1)反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H1,平衡常数为K1;反应Fe(s)+H2O(g)?FeO(s)+H2(g)△H2,平衡常数为K2.在不同温度时K1、K2的值如表:
(1)反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H1,平衡常数为K1;反应Fe(s)+H2O(g)?FeO(s)+H2(g)△H2,平衡常数为K2.在不同温度时K1、K2的值如表:
①反应 CO2(g)+H2(g)?CO(g)+H2O(g)△H,平衡常数K,则△H=△H1-△H2(用△H1和△H2表示),K=$\frac{{K}_{1}}{{K}_{2}}$(用K1和K2表示),且由上述计算可知,反应CO2(g)+H2(g)?CO(g)+H2O(g)是吸热反应(填“吸热”或“放热”).
(2)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H>0,CO2的浓度与时间的关系如图所示:
①该条件下反应的平衡常数为2.0;
②下列措施中能使平衡时$\frac{c(CO)}{c(C{O}_{2})}$增大的是A(填序号)
A.升高温度 B.增大压强
C.充入一定量的CO2 D.再加入一定量铁粉
③一定温度下,在一个固定容积的密闭容器中发生上述反应,下列能判断该反应达到化学平衡状态的是bc(填字母).
a.容器中压强不变 b.气体的密度不再改变c.v正(CO2)=v逆(CO) d.c(CO2)=c(CO) e.容器内气体总物质的量不变.
 (1)反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H1,平衡常数为K1;反应Fe(s)+H2O(g)?FeO(s)+H2(g)△H2,平衡常数为K2.在不同温度时K1、K2的值如表:
(1)反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H1,平衡常数为K1;反应Fe(s)+H2O(g)?FeO(s)+H2(g)△H2,平衡常数为K2.在不同温度时K1、K2的值如表:| 700℃ | 900℃ | |
| K1 | 1.47 | 2.15 |
| K2 | 2.38 | 1.67 |
(2)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H>0,CO2的浓度与时间的关系如图所示:
①该条件下反应的平衡常数为2.0;
②下列措施中能使平衡时$\frac{c(CO)}{c(C{O}_{2})}$增大的是A(填序号)
A.升高温度 B.增大压强
C.充入一定量的CO2 D.再加入一定量铁粉
③一定温度下,在一个固定容积的密闭容器中发生上述反应,下列能判断该反应达到化学平衡状态的是bc(填字母).
a.容器中压强不变 b.气体的密度不再改变c.v正(CO2)=v逆(CO) d.c(CO2)=c(CO) e.容器内气体总物质的量不变.
5.醋酸是一种常见的一元弱酸,为了证明醋酸是弱电解质,某同学开展了题为“醋酸是弱电解质”的实验探究活动.该同学设计了如下方案,其中错误的是( )
| A. | 先配制一定量的0.10mol/LCH3COOH溶液,然后测溶液的c(H+),若c(H+)小于0.10mol/L,则可证明醋酸为弱电解质 | |
| B. | 先配制一定量0.0010mol•L-1和0.10mol•L-1的CH3COOH,分别用pH计测它们的c(H+),若前者的c(H+)与后者c(H+)的比值小于10,则可证明醋酸是弱电解质 | |
| C. | 取等体积、等c(H+)的CH3COOH溶液和盐酸分别于足量等规格的锌粒反应,若反应过程中醋酸产生H2较慢且最终产生H2较多,则可证明醋酸是弱电解质 | |
| D. | 取等体积、等c(H+)的CH3COOH溶液和盐酸分别加水稀释相同的倍数,若稀释后CH3COOH溶液中c(H+)大,则可证明醋酸是弱电解质 |

 (1)在一定条件下N2和H2完全反应生成1molNH3放热46.0kJ热量.写出氨分解为氢气和氮气的热化学方程式2NH3(g)=N2(g)+3H2(g)△H=+92KJ/mol
(1)在一定条件下N2和H2完全反应生成1molNH3放热46.0kJ热量.写出氨分解为氢气和氮气的热化学方程式2NH3(g)=N2(g)+3H2(g)△H=+92KJ/mol