题目内容
6.Mn2+、Bi3+、BiO3-、MnO4-、H+、H2O组成的一个氧化还原反应体系中,发生BiO3-→Bi3+的反应过程,据此回答下列问题:将以上物质分别填入下面对应的横线上,组成一个为配平的化学方程式.
2Mn2++5BiO3-+14H+→2MnO4-+5Bi3++7H2O.
分析 发生BiO3-→Bi3+的反应,Bi元素由+5价降低为+3价即发生还原反应,一个氧化还原反应体系则还要发生氧化反应即Mn2+→MnO4-,Mn元素由+2升高为+7,发生Mn2++BiO3-+H+→MnO4-+Bi3++H2O,结合电子守恒及质量守恒定律来配平.
解答 解:发生BiO3-→Bi3+的反应,Bi元素由+5价降低为+3价即发生还原反应,一个氧化还原反应体系则还要发生氧化反应即Mn2+→MnO4-,Mn元素由+2升高为+7,发生Mn2++BiO3-+H+→MnO4-+Bi3++H2O,由电子守恒及质量守恒定律可知,该反应为2Mn2++5BiO3-+14H+═2MnO4-+5Bi3++7H2O,
故答案为:2Mn2+;5BiO3-;14H+;2MnO4-;5Bi3+.
点评 本题考查氧化还原反应,明确反应中元素的化合价变化即可解答,题目难度不大.

练习册系列答案
相关题目
16.阿斯巴甜是目前使用最广泛的甜味剂.甜度约为蔗糖的200倍,其结构简式为:
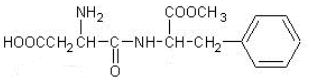
下列关于阿斯巴甜的说法正确的是( )

下列关于阿斯巴甜的说法正确的是( )
| A. | 分子式为C14H19N2O5 | B. | 既能与酸反应又能与碱反应 | ||
| C. | 不能发生水解反应 | D. | 1mol该物质最多可与2molNaOH反应 |
17.下列离子方程式中正确的是( )
| A. | 氯气通入冷水中:Cl2+H2O?Cl-+ClO-+2H+ | |
| B. | 亚硫酸氨溶液与足量氢氧化钠溶液反应 HSO3-+OH-═SO32-+H2O | |
| C. | 氢氧化钠溶液吸收过量的二氧化碳 OH-+CO2═HCO3- | |
| D. | 碳酸镁悬浊液中加醋酸 CO32-+2CH3COOH═2CH3COO-+CO2↑+H2O |
14.下列物质在自然界中能稳定存在的是( )
| A. | 过氧化钠 | B. | 氧化钠 | C. | 碳酸钠 | D. | 氢氧化钠 |
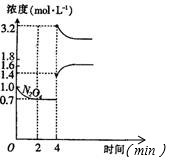
 氰、硫、碳的氧化物有多种,其中S02和N0x都是大气污染物,对它们的研究有助于空气的净化.
氰、硫、碳的氧化物有多种,其中S02和N0x都是大气污染物,对它们的研究有助于空气的净化.