题目内容
3.若在NaClO3浓溶液中加入固体KCl,则可得到重要化工产品KClO3晶体.下述有关生产原理正确的是( )| A. | 变化的化学方程式是:NaCl03+KCl=KClO3(结晶)+NaCl | |
| B. | KClO3是难溶物 | |
| C. | KClO3是比NaClO3更弱的电解质 | |
| D. | 相同温度下,KCl03的溶解度比NaCl03小 |
分析 若在NaClO3浓溶液中加入固体KCl,则可得到重要化工产品KClO3晶体,方程式为:NaCl03+KCl=KClO3(结晶)+NaCl,依据复分解反应的条件可知该反应能发生与Ca(ClO3)2、KClO3的溶解度有关,据此解答.
解答 解:相同温度下,KCl03的溶解度比NaCl03小,依据复分解反应的条件可知:NaCl03+KCl=KClO3(结晶)+NaCl能够发生,即在NaClO3浓溶液中加入固体KCl,则可得到重要化工产品KClO3晶体,而氯酸钾为钾盐,易溶于水,氯酸钾、氯酸钠都是可溶性盐,在水溶液中能够完全电离,都是强电解质,
故选:AD.
点评 本题考查了复分解反应条件,电解质、非电解质判断,明确反应原理及基本概念即可解答,题目难度不大.

练习册系列答案
相关题目
14.下列物质属于电解质的是( )
| A. | 蔗糖 | B. | 玻璃 | C. | 纯碱 | D. | 铁 |
11.常温下,0.1mol/L的硫酸铜溶液里,各离子浓度大小的顺序正确的是( )
| A. | c(OH-)<c(Cu2+)<c(H+)<c(SO42-) | B. | c(OH-)<c(H+)<c(SO42-)<c(Cu2+) | ||
| C. | c(OH-)<c(H+)<c(SO42-)=c(Cu2+) | D. | c(OH-)<c(H+)<c(Cu2+)<c(SO42-) |
8.化学与社会、生产、生活密切相关,下列说法正确的是( )
| A. | 金属钠、碳化钙着火时,可直接用高压水枪喷火扑灭 | |
| B. | 去除银器表面的Ag2S,可将银器放在盛有食醋的铝锅中煮沸 | |
| C. | 苹果在空气中久置变黄和纸张变黄的原理相似 | |
| D. | 用乙醚从黄花蒿中萃取青蒿素发生了氧化还原反应 |
15.乳酸的结构简式如图,对乳酸的化学性质推测不正确的是( )
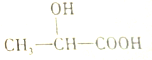
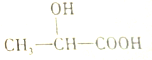
| A. | 1mol乳酸可以与足量的NaHCO3反应生成1molCO2 | |
| B. | 1mol乳酸可以与足量的钠反应生成1mol氢气 | |
| C. | 乳酸可以在一定条件下发生消去反应生成CH2=CHCOOH | |
| D. | 乳酸可以与NaOH溶液反应生成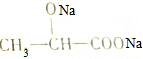 |
14.酸性KMnO4溶液能与草酸(H2C2O4)溶液反应.某探究小组利用反应过程中溶液紫色消失快慢的方法来研究影响反应速率的因素.
Ⅰ.实验前首先用浓度为0.1000mol•L-1酸性KMnO4标准溶液滴定未知浓度的草酸.
(1)写出滴定过程中发生反应的化学方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O.
(2)滴定过程中操作滴定管的图1示正确的是A.
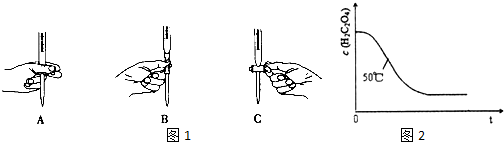
(3)若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的草酸溶液浓度偏高(填“偏高”、“偏低”、或“不变”).
Ⅱ.通过滴定实验得到草酸溶液的浓度为0.2000mol•L-1.用该草酸溶液按下表进行后续实验(每次实验草酸溶液的用量均为8mL).
(4)写出表中a 对应的实验目的探究温度不同对反应速率的影响;若50℃时,草酸浓度c(H2C2O4)随反应时间t的变化曲线如图2所示,保持其他条件不变,请在图中画出25℃时c(H2C2O4)随t的变化曲线示意图.
(5)该小组同学对实验1和3分别进行了三次实验,测得以下实验数据(从混合振荡均匀开始计时):
分析上述数据后得出“当其它条件相同时,酸性高锰酸钾溶液的浓度越小,褪色时间就越短,即反应速率就越快”的结论.甲同学认为该小组“探究反应物浓度对速率影响”的实验方案设计中存在问题,从而得到了错误的实验结论,请简述甲同学改进的实验方案其它条件相同时,利用等量且少量的高锰酸钾与等体积不同浓度的足量草酸溶液反应,测量溶液褪色时间.
(6)该实验中使用的催化剂应选择MnSO4而不是MnCl2,原因可用离子方程式表示为2MnO4-+10Cl-+16H+=5Cl2↑+2Mn2++8H2O.
Ⅰ.实验前首先用浓度为0.1000mol•L-1酸性KMnO4标准溶液滴定未知浓度的草酸.
(1)写出滴定过程中发生反应的化学方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O.
(2)滴定过程中操作滴定管的图1示正确的是A.

(3)若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的草酸溶液浓度偏高(填“偏高”、“偏低”、或“不变”).
Ⅱ.通过滴定实验得到草酸溶液的浓度为0.2000mol•L-1.用该草酸溶液按下表进行后续实验(每次实验草酸溶液的用量均为8mL).
| 实验编号 | 温度(℃) | 催化剂 用量(g) | 酸性高锰酸钾溶液 | 实验目的 a.实验1和2探究探究温度不同对反应速率的影响; b.实验1和3探究反应物浓度对该反应速率的影响; c.实验1和4探究催化剂对该反应速率的影响. | |
| 体积 (mL) | 浓度 (mol•L-1) | ||||
| 1 | 25 | 0.5 | 4 | 0.1000 | |
| 2 | 50 | 0.5 | 4 | 0.1000 | |
| 3 | 25 | 0.5 | 4 | 0.0100 | |
| 4 | 25 | 0 | 4 | 0.1000 | |
(5)该小组同学对实验1和3分别进行了三次实验,测得以下实验数据(从混合振荡均匀开始计时):
| 实验编号 | 溶液褪色所需时间(min) | ||
| 第1次 | 第2次 | 第3次 | |
| 1 | 14.0 | 13.0 | 11.0 |
| 3 | 6.5 | 6.7 | 6.8 |
(6)该实验中使用的催化剂应选择MnSO4而不是MnCl2,原因可用离子方程式表示为2MnO4-+10Cl-+16H+=5Cl2↑+2Mn2++8H2O.

 .
.