题目内容
11.10mL pH=4的盐酸中,加水至100mL时,pH=5.分析 pH=-lgc(H+),可知pH=4的盐酸中,c(H+)=10-4mol/L,根据溶液稀释前后溶质的物质的量不变,计算稀释后的c(H+),进而计算pH.
解答 解:pH=4的盐酸中,c(H+)=10-4mol/L,
10mL pH=4的盐酸中,加水至100mL时,c(H+)=10-5mol/L,
pH=-lg10-5=5,
故答案为:5.
点评 本题考查了pH的简单计算,为高频考点,侧重于学生的分析、计算能力的考查,答题时注意先计算溶液中氢离子浓度,再根据PH公式进行计算,题目难度不大.

练习册系列答案
相关题目
2.某反应的反应物X浓度在20s内由1.0mol•L-1变成了0.2mol•L-1,则以X浓度的变化表示的该反应在这段时间内的平均反应速率为( )
| A. | 0.04mol•L-1 | B. | 0.04mol•L-1•s-1 | C. | 0.08mol•L-1 | D. | 0.08mol•L-1•s-1 |
3.鉴别下列各组物质,选用的试剂或方法错误的是( )
| 选项 | 要鉴别的物质组 | 试剂 | 方法 |
| A | NaCl/Na2CO3 | BaCl2溶液 | 观察是否产生沉淀 |
| B | NO2/Br2 | 湿润的淀粉碘化钾试纸 | 观察试纸是否变蓝色 |
| C | 乙醇/乙酸 | 新制氢氧化铜悬浊液 | 观察溶液是否变澄清 |
| D | CO2/SO2 | 品红溶液 | 观察溶液红色是否退去 |
| A. | A | B. | B | C. | C | D. | D |
12.一定体积的甲烷在一定量O2中燃烧得到产物为CO,CO2和水蒸气,测得混合气体的质量为49.6g,将混合气体缓慢通过无水CaCl2时,CaCl2质量增加25.2g,则混合气体中CO2的质量为( )
| A. | 12.5g | B. | 13.2g | C. | 19.7g | D. | 24.4g |
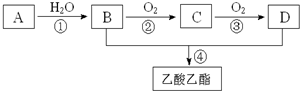
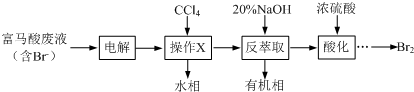
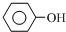 +3Br2→
+3Br2→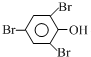 ↓+3HBr
↓+3HBr